题目内容
2.海水中含有丰富的氯化镁.如图是从海水中提取镁的简单流程.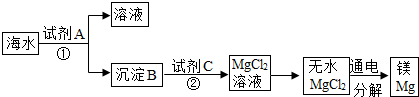
(1)上述提取Mg的过程中,试剂A最好选用Ca(OH)2.沉淀B与试剂C发生的是中和反应,则沉淀B的化学式为Mg(OH)2.
(2)电解无水MgCl2可制取Mg,试写出相关的化学方程式MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑.
分析 (1)氯化镁转化为氢氧化镁需要加入碱液,验证MgCl2已完全转化为Mg(OH)2的方法是取滤液滴入Ca(OH)2溶液是否有沉淀生成;
(2)利用题目所给的信息结合书写化学方程式的原则进行书写.
解答 解:(1)氯化镁转化为氢氧化镁需要加入碱液以提供氢氧根,此处选择过量的氢氧化钙进行反应,目的是让所取海水中的氯化镁全部转化为氢氧化镁沉淀;
故填:Ca(OH)2;Mg(OH)2;
(2)由题中可知反应产物,再结合化学反应方程式的书写原则书写方程式.故答案为:MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑;故填:MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑.
点评 化学来源于生产、生活,又服务于生产、生活,用海水来制备金属镁是初中化学重要的应用之一,是考查重点,常涉及化学方程式的书写.

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
12.除去下列物质中所含的少量杂质,方法正确的是( )
| 物 质 | 所含杂质 | 除杂质的方法 |
| A.二氧化锰 | 氯化钠 | 加水溶解,过滤,蒸发结晶 |
| B.氯化钠固体 | 碳酸钠 | 加入过量稀盐酸,蒸发结晶 |
| C.氯化钙溶液 | 稀盐酸 | 加入过量氢氧化钙,过滤 |
| D.氢氧化钠溶液 | 碳酸钠 | 加入适量的石灰水、过滤 |
| A. | A | B. | B | C. | C | D. | D |
10.水华现象是在特定的环境条件下,海水中某些浮游植物、原生动物或细菌爆发性增殖或高度聚集而引起水体变色的一种有害生态现象.大量工农业废水和生活污水排入海洋,其中相当一部分未经处理就直接排入海洋,导致近海、港湾富营养化程度日趋严重.对湖泊出现的“水华”现象,下列叙述不正确的是( )
| A. | 生活污水不经处理排入湖泊,容易引发藻类过度繁殖 | |
| B. | 湖水温度升高是引起藻类大量繁殖的主要因素 | |
| C. | 藻类植物过度繁殖,会破坏湖泊原有生态系统 | |
| D. | 藻类植物过度繁殖可导致鱼虾死亡 |
14.逻辑推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | 中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应 | |
| B. | 因为MnO2能加快H202的分解,所以催化剂一定加快化学反应速度 | |
| C. | 化合物由不同种元素组成,所以由不同元素组成的纯净物一定是化合物 | |
| D. | 碱的水溶液通常呈碱性,所以呈碱性的溶液一定是碱溶液 |
11.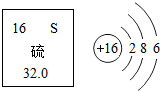 如图是硫元素的部分信息及硫原子的结构示意图.关于硫元素的有关说法不正确的是( )
如图是硫元素的部分信息及硫原子的结构示意图.关于硫元素的有关说法不正确的是( )
 如图是硫元素的部分信息及硫原子的结构示意图.关于硫元素的有关说法不正确的是( )
如图是硫元素的部分信息及硫原子的结构示意图.关于硫元素的有关说法不正确的是( )| A. | 硫化钠的相对原子质量为55 | |
| B. | 一个硫酸分子由7个原子构成 | |
| C. | 二氧化硫中硫元素的质量分数为50% | |
| D. | 硫原子核外共有16个电子,最外层有6个电子 |
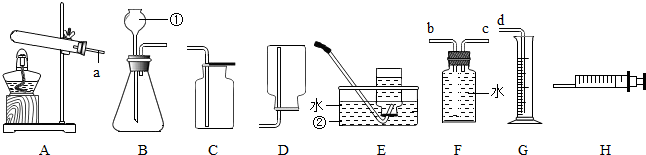
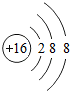 表示的粒子S2-;
表示的粒子S2-;