题目内容
7.将20g锌粒投入73g未知浓度的盐酸中,当反应停止后,溶液中尚有锌粒剩余,过滤后,滤液的质量为85.6g,求该盐酸的质量分数.分析 锌与稀盐酸反应生成氯化锌和氢气,反应停止后,溶液中尚有锌粒剩余,由题意,过滤后,滤液的质量为85.6g,则反应后溶液的质量增加了85.6g-73g=12.6g;由液体差量法,进行分析解答即可.
解答 解:设参加的稀盐酸中溶质的质量为x
Zn+2HCl═ZnCl2+H2↑ 溶液质量增加
73 136 136-73=63
x 85.6g-73g=12.6g
$\frac{73}{63}$=$\frac{x}{12.6g}$ x=14.6g
该盐酸的质量分数为$\frac{14.6g}{73g}$×100%=20%.
答:该盐酸的质量分数为20%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
18. 金属材料与人类的生产和生活密切相关.
金属材料与人类的生产和生活密切相关.
2015年5月12日,海西高速公路网的重要组成部分:福建省最长跨海大桥-泉州湾大桥正式通车.大桥的建设及通行涉及到许多的化学知识.
(1)制造大桥护栏和斜拉索等重要器件的材料都是钢,钢属于金属(选填“金属”或“无机非金属”)材料.
(2)工人给大桥钢铁器件喷上油漆,目的是为了防止铁与O2、H2O发生反应而生锈.
(3)A、B、C、D四中金属单质,A能从B的化合物溶液中置换出B,但A不能与稀盐酸反应.相同条件下,C、D能与稀盐酸反应产生氢气,且D比C反应剧烈.则四种金属的活动性由强到弱的顺序是:D>C>A>B.
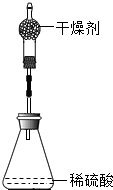
(4 )锌铜合金中是铜合金中的一种,用途较为广泛.为测定锌铜合金中锌的含量,取该合金放入如图盛有稀硫酸的锥形瓶中,发生反应:Zn+H2SO4═ZnSO4+H2↑.多次实验后,取平均值所得数据如表:
若不考虑干燥剂吸收空气中的水蒸气,计算:
ⅰ根据质量守恒定律求生成氢气的质量是多少g?
ⅱ该合金中锌的质量分数是多少?(请写出计算过程)
 金属材料与人类的生产和生活密切相关.
金属材料与人类的生产和生活密切相关.2015年5月12日,海西高速公路网的重要组成部分:福建省最长跨海大桥-泉州湾大桥正式通车.大桥的建设及通行涉及到许多的化学知识.
(1)制造大桥护栏和斜拉索等重要器件的材料都是钢,钢属于金属(选填“金属”或“无机非金属”)材料.
(2)工人给大桥钢铁器件喷上油漆,目的是为了防止铁与O2、H2O发生反应而生锈.
(3)A、B、C、D四中金属单质,A能从B的化合物溶液中置换出B,但A不能与稀盐酸反应.相同条件下,C、D能与稀盐酸反应产生氢气,且D比C反应剧烈.则四种金属的活动性由强到弱的顺序是:D>C>A>B.
(4 )锌铜合金中是铜合金中的一种,用途较为广泛.为测定锌铜合金中锌的含量,取该合金放入如图盛有稀硫酸的锥形瓶中,发生反应:Zn+H2SO4═ZnSO4+H2↑.多次实验后,取平均值所得数据如表:
| 反应前 | 充分反应后装置及反应剩余物质质量 | |
| 装置和足量的稀硫酸质量 | 锌铜合金质量 | |
| 342.10g | 16.00g | 357.70g |
ⅰ根据质量守恒定律求生成氢气的质量是多少g?
ⅱ该合金中锌的质量分数是多少?(请写出计算过程)
2.某实验小组的同学用氢氧化钠溶液和硫酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液加入稀硫酸一会后,实验中未观察到明显现象.他们停止滴加稀硫酸,并对烧杯内溶液中的溶质成分进行探究.
(1)写出该中和反应的化学方程式:H2SO4+2NaOH═Na2SO4+2H2O;
【提出问题】该烧杯内溶液中的溶质是什么.
【猜想】猜想Ⅰ:有Na2SO4和NaOH;
猜想Ⅱ:有Na2SO4和H2SO4;
猜想Ⅲ:Na2SO4;
【查阅资料】①BaCl2、Na2SO4溶液显中性,且Ba2+有毒.
【实验探究】小组同学取烧杯中的溶液少量于试管中,进行如下两个方案的探究.
[得出结论】(1)为什么会出现截然不同的结论呢?同学们经过检查,发现操作准确无误,讨论后同学一致认定猜想Ⅰ正确.另一结论错误的原因是Na2SO4+BaCl2═BaSO4↓+2NaCl.(用化学方程式表示)
【反思拓展】(1)实验结束了,小组同学将所有废液倒进废液缸,为了除去废液中的有害成分并将废液调至中性,应向废液缸中加入适量的稀硫酸.
(2)根据所学化学知识,验证烧杯内溶液中的溶质是否含有H2SO4,除以上方案外,单独使用某种试剂也能完成该实验,你选用的一种试剂是石蕊试液.
(1)写出该中和反应的化学方程式:H2SO4+2NaOH═Na2SO4+2H2O;
【提出问题】该烧杯内溶液中的溶质是什么.
【猜想】猜想Ⅰ:有Na2SO4和NaOH;
猜想Ⅱ:有Na2SO4和H2SO4;
猜想Ⅲ:Na2SO4;
【查阅资料】①BaCl2、Na2SO4溶液显中性,且Ba2+有毒.
【实验探究】小组同学取烧杯中的溶液少量于试管中,进行如下两个方案的探究.
| 实验方案 | 测溶液pH | 滴加过量BaCl2溶液 |
| 实验现象 | pH=10 | 产生白色沉淀 |
| 实验结论 | 溶液中有NaOH | 溶液中有H2SO4 |
【反思拓展】(1)实验结束了,小组同学将所有废液倒进废液缸,为了除去废液中的有害成分并将废液调至中性,应向废液缸中加入适量的稀硫酸.
(2)根据所学化学知识,验证烧杯内溶液中的溶质是否含有H2SO4,除以上方案外,单独使用某种试剂也能完成该实验,你选用的一种试剂是石蕊试液.
12.下列有关说法正确的是( )
| A. | 塑料给环境带来了污染,因此要全面禁止生产和使用 | |
| B. | 煤和石油属于不可再生能源 | |
| C. | 催化剂只能加快化学反应的速率 | |
| D. | 铁、碘、钙是人体必需的微量元素 |
19.某方便面的营养成分表如表(其中碳水化合物主要指淀粉等):
(1)表中“钠”是指C(填序号).
A.离子 B.分子 C.元素 D.单质
(2)方便面中含的营养素有4种.
(3)方便面中使用的食盐可以是加碘盐,人体中缺碘可能患有的疾病是甲状腺肿大(填“甲状腺肿大”或“骨质疏松”).
(4)若小明用天然气煮方便面,请问天然气主要成份燃烧的化学方程式是CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
| 营 养 成 分 表 |
| 项目 每100克 |
| 能量 1966千焦 蛋白质 7.5克 脂肪 21.8克 碳水化合物 60.7克 钠 2530毫克 |
A.离子 B.分子 C.元素 D.单质
(2)方便面中含的营养素有4种.
(3)方便面中使用的食盐可以是加碘盐,人体中缺碘可能患有的疾病是甲状腺肿大(填“甲状腺肿大”或“骨质疏松”).
(4)若小明用天然气煮方便面,请问天然气主要成份燃烧的化学方程式是CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
17.太空舱利用铁酸镍(NiFe2O4)将航天员呼出的二氧化碳转化为氧气,而铁酸镍的质量和化学性质反应前后都不变.下列有关铁酸镍的说法正确的是( )
| A. | 属于酸 | B. | 镍、铁、氧三种元素质量比是1:2:4 | ||
| C. | 铁元素化合价为+3,则镍元素为+2 | D. | 铁酸镍在该化学变化中是反应物 |
