题目内容
实验室里为制取等质量的铜,有下列两个途径:
(1)Fe
H2
Cu
(2)CuO
CuSO4
Cu
①消耗相同质量的CuO②消耗相同质量的Fe③消耗相同质量的稀H2SO4④生成不同质量的FeSO4,其中符合实际情况的是( )
(1)Fe
| 稀H2SO4 |
| ||
| △ |
(2)CuO
| 稀H2SO4 |
| Fe |
①消耗相同质量的CuO②消耗相同质量的Fe③消耗相同质量的稀H2SO4④生成不同质量的FeSO4,其中符合实际情况的是( )
| A、①② | B、①④ |
| C、①②③ | D、②③④ |
分析:根据氢气还原氧化铜的实验步骤和注意事项可知,要通入氢气一段时间,然后再加热反应,其目的是排出里面的空气,防止爆炸.
解答:解:第一种方案:Fe+H2SO4=FeSO4+H2↑,H2+CuO
Cu+H2O.根据氢气还原氧化铜的实验注意事项可知,氢气要通入一段时间后才开始加热反应,因此氢气是过量的.所以生成64克铜需要氧化铜的质量等于80克,需要氢气的质量大于2克;生成大于2克的氢气需要铁的质量大于56克,需要硫酸的质量大于98克,同时生成硫酸亚铁的质量大于152克.
第二种方案:CuO+H2SO4=CuSO4+H2O,CuSO4+Fe=FeSO4+Cu.说明生成64克铜需要56克铁和160克硫酸铜,同时生成硫酸亚铁的质量为152克;生成160克硫酸铜需要80克氧化铜和98克硫酸.综合上述分析可知,①④叙述正确,故选B.
| ||
第二种方案:CuO+H2SO4=CuSO4+H2O,CuSO4+Fe=FeSO4+Cu.说明生成64克铜需要56克铁和160克硫酸铜,同时生成硫酸亚铁的质量为152克;生成160克硫酸铜需要80克氧化铜和98克硫酸.综合上述分析可知,①④叙述正确,故选B.
点评:本题的关键是知道氢气还原氧化铜实验的操作方法,即氢气是过量,所以需要硫酸和铁的质量也过量,因此可以排除②③,从而得到正确答案.

练习册系列答案
相关题目
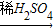 H2
H2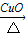 Cu
Cu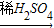 CuSO4
CuSO4 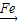 Cu
Cu