题目内容
 如图是电解水的实验装置图,请根据你所了解的知识填空:
如图是电解水的实验装置图,请根据你所了解的知识填空:(1)A为
(2)电解1mol水产生O2的物质的量为多少?(写出计算过程)
分析:(1)根据电解水的实验现象回答.
(2)根据化学方程式计算时,按照设,方,关,比,算,答的步骤进行.
(2)根据化学方程式计算时,按照设,方,关,比,算,答的步骤进行.
解答:解:(1)电解水时,负极产生氢气,正极产生氧气,氢气和氧气的体积比是2:1,从图示看出,A极产生的气体体积大,故为氢气,那么A就为 负极;
(2)根据电解水的化学方程式,有摩尔量的比可计算出氧气的摩尔质量.
答案:(1)负极
(2)解设产生氧气的物质的量为x
2H2O
2H2↑+O2↑
2 1
1mol x
=
x=0.5 mol
答:产生的O2物质的量为0.5mol
(2)根据电解水的化学方程式,有摩尔量的比可计算出氧气的摩尔质量.
答案:(1)负极
(2)解设产生氧气的物质的量为x
2H2O
| ||
2 1
1mol x
| 2 |
| 1 |
| 1 |
| x |
x=0.5 mol
答:产生的O2物质的量为0.5mol
点评:同学们要按步骤规范的解答根据化学方程式的计算,减少不必要的失分.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
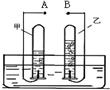 如图是电解水的实验装置图,请根据你所了解的知识填空:
如图是电解水的实验装置图,请根据你所了解的知识填空: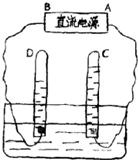 如图是电解水的实验装置图,请根据图回答:
如图是电解水的实验装置图,请根据图回答: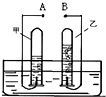 如图是电解水的实验装置图,请根据你所了解的知识填空:
如图是电解水的实验装置图,请根据你所了解的知识填空: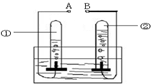 如图是电解水的实验装置图,请根据图和题意回答问题:
如图是电解水的实验装置图,请根据图和题意回答问题: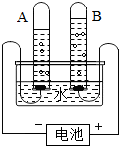 水是生命之源.请回答:
水是生命之源.请回答: