题目内容
7.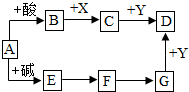 下图是初中化学常见物质间的转化关系(反应条件和部分产物已略去),其中A为含有三种元素的钠盐;X、Y均为黑色粉末;D为红色金属单质;F在常温下为液态.
下图是初中化学常见物质间的转化关系(反应条件和部分产物已略去),其中A为含有三种元素的钠盐;X、Y均为黑色粉末;D为红色金属单质;F在常温下为液态.(1)则A的化学式是Na2CO3.
(2)写出C→D的化学方程式CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
(3)若E→F为中和反应,则E的化学式为NaOH.
(4)写出上述物质转化过程中,属于分解反应的化学方程式2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
分析 A为含有三种元素的钠盐;X、Y均为黑色粉末;D为红色金属单质,则D为铜,可推出Y是黑色粉末CuO;将氧化铜变为红色铜的物质常见的是CO、氢气和碳,X为黑色粉末,X为碳单质,则C为一氧化碳,二氧化碳与碳反应生成一氧化碳,则B为二氧化碳,A是碳酸盐,则A为碳酸钠;F常温下为液态,且生成了可以氧化铜反应的G,可以判断G为氢气,而F为水;据此进行分析解答.
解答 解:A为含有三种元素的钠盐;X、Y均为黑色粉末;D为红色金属单质,则D为铜,可推出Y是黑色粉末CuO;将氧化铜变为红色铜的物质常见的是CO、氢气和碳,X为黑色粉末,X为碳单质,则C为一氧化碳,二氧化碳与碳反应生成一氧化碳,则B为二氧化碳,A是碳酸盐,则A为碳酸钠;F常温下为液态,且生成了可以氧化铜反应的G,可以判断G为氢气,而F为水.
(1)A为碳酸钠,其化学式为:Na2CO3.
(2)C→D,即一氧化碳与氧化铜反应生成铜和二氧化碳,反应的化学方程式为:CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
(3)E→F为中和反应,则应为碳酸钠与氢氧化钙反应生成的氢氧化钠与稀盐酸(或稀硫酸等)反应,E的化学式为NaOH.
(4)分解反应:一种物质反应后生成两种或两种以上的物质,其特点可总结为“一变多”,题中只有水分解制氢气的反应属于分解反应,水通电分解生成氢气和氧气,反应的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
故答案为:(1)Na2CO3;(2)CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;(3)NaOH;(4)2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
点评 本题难度不大,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证.

 阅读快车系列答案
阅读快车系列答案| A. | 氧气可用于医疗急救 | B. | 干冰可用于人工降雨 | ||
| C. | 液氧养用于火箭的助燃剂 | D. | 二氧化碳作气体肥料 |
| 指示剂 (花汁) | 在不同溶液中的颜色变化 | ||||
| 盐酸 | 酒精溶液 | 氢氧化钠溶液 | 石灰水 | ||
| A | 红玫瑰 | 粉红色 | 粉红色 | 绿色 | 绿色 |
| B | 万寿菊 | 黄色 | 黄色 | 黄色 | 黄色 |
| C | 月季花 | 浅红色 | 红色 | 黄色 | 黄色 |
| D | 丝瓜花 | 红色 | 红色 | 黄绿色 | 黄绿色 |
| A. | A | B. | B | C. | C | D. | D |
| 事 实 | 解 释 | |
| A | 氧气用于切割金属 | 氧气有可燃性 |
| B | 洗洁精可用于除油污 | 洗洁精能溶解油污 |
| C | 打开汽水瓶盖有大量气泡冒出 | 温度升高,气体溶解度减小 |
| D | 做铁丝燃烧实验时集气瓶底部预先要装少量的水 | 防止瓶底炸裂 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 推广使用LED节能灯 | B. | 大力发展沼气 | ||
| C. | 加快煤炭综合利用的步伐 | D. | 大力发展火力发电 |
| A. |  滴加液体 | B. |  闻气味 | C. |  量筒读数 | D. |  熄灭酒精灯 |
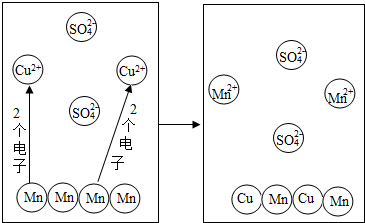 从微观的角度了解物质及其变化,有助于更好的认识物质组成和变化的本质.
从微观的角度了解物质及其变化,有助于更好的认识物质组成和变化的本质.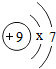 ,则x=2,在化学反应中氟原子易得到(填“得到”或“失去“)电子.
,则x=2,在化学反应中氟原子易得到(填“得到”或“失去“)电子.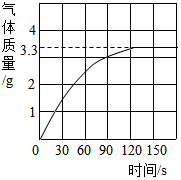 某化学兴趣小组的同学欲测定一定质量的大理石样品中碳酸钙的质量,将100g足量的稀盐酸加入到装有l0g大理石(研成粉末)的烧杯中(杂质与盐酸不反应),同时测量150s内产生的气体的质量变化,反应时间与产生气体的质量如图所示.
某化学兴趣小组的同学欲测定一定质量的大理石样品中碳酸钙的质量,将100g足量的稀盐酸加入到装有l0g大理石(研成粉末)的烧杯中(杂质与盐酸不反应),同时测量150s内产生的气体的质量变化,反应时间与产生气体的质量如图所示.