题目内容
19. 【发现问题】研究性学习小组中的小张同学在学习中发现:通常检验CO2用饱和石灰水;吸收CO2用浓NaOH溶液.
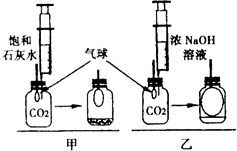
【发现问题】研究性学习小组中的小张同学在学习中发现:通常检验CO2用饱和石灰水;吸收CO2用浓NaOH溶液.【实验探究】在体积相同盛满CO2的两集气瓶中,
分别加入等体积的饱和石灰水和浓NaOH溶液.
实验装置和现象如右图所示.
【现象结论】甲装置中产生的实验现象产生白色沉淀,通常用石灰水而不用NaOH溶液检验CO2的原因二氧化碳与氢氧化钙反应现象明显,与氢氧化钠反应没有明显现象;乙装置中的实验现象是气球胀大,吸收CO2较多的装置是乙,所以吸收CO2用浓NaOH溶液.
分析 根据二氧化碳能和石灰水反应生成碳酸钙沉淀和水,氢氧化钠能和二氧化碳反应生成易溶于水的碳酸钠和水,氢氧化钙在水中的溶解度小,氢氧化钠在水中的溶解度大进行分析.
解答 解:氢氧化钙和二氧化碳反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O,通常用石灰水而不用NaOH 溶液检验CO2的原因是:CO2与石灰水作用有明显实验现象,与NaOH作用无明显现象,乙装置中的实验现象是:气球体积增大,溶液不变浑浊,由气球膨胀的程度可以推知,氢氧化钠吸收的二氧化碳较多.
故答案为:产生白色沉淀,二氧化碳与氢氧化钙反应现象明显,与氢氧化钠反应没有明显现象,气球胀大,乙.
点评 解答本题要从氢氧化钙、氢氧化钠与二氧化碳相互作用时的实验现象、氢氧化钙和氢氧化钠的溶解度等方面进行分析、判断,从而得出正确的结论.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
9.下列有关认识正确的是( )
| A. | 用石墨可制得金刚石 | B. | “绿色食品”就是绿颜色的食品 | ||
| C. | 稀有气体不与任何物质反应 | D. | 纯牛奶中不含任何物质 |
14.下列变化属于化学变化的是( )
| A. | 煤隔绝空气加热变成焦炭等物质 | B. | 活性炭吸附水中色素 | ||
| C. | 石油分离得到汽油、柴油等物质 | D. | 自行车轮胎爆炸 |
4. 某化学兴趣小组的同学设计了如下实验来验证二氧化碳气体的相关性质,实验步骤如下:
某化学兴趣小组的同学设计了如下实验来验证二氧化碳气体的相关性质,实验步骤如下:
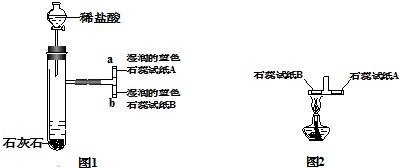
Ⅰ.取一个三通管(三个管口都未密封,与空气相通),在三通管的上部和下部各放一张湿润的蓝色石蕊试纸(湿润的蓝色石蕊试纸遇到酸性物质会变红).然后将它与二氧化碳的发生装置连接.(如图1,整套装置的气密性良好)
Ⅱ.打开分液漏斗的活塞,使石灰石与稀盐酸接触,观察到相关现象后,停止实验.
Ⅲ.取下图1中的三通管,把贴有试纸B的那端放在酒精灯火焰上加热(如图2),
观察实验现象.
注:整个实验中不考虑反应过程中水分和HCl气体的挥发,且图1中产生的气流较缓慢
根据上述实验,回答下列问题:
(1)实验Ⅱ步骤中三通管内产生的实验现象是b处湿润的蓝色湿润试纸变红;由此说明二氧化碳气体具有二氧化碳密度大于空气、二氧化碳能与水反应的性质.
(2)实验Ⅲ步骤中一定发生的化学反应方程式是H2CO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2↑;
(3)若不改变图1的实验装置,还要验证二氧化碳气体具有不能燃烧、也不能支持燃烧的性质,需要补充的实验是取一根燃着的小木条放在b导管口,发现小木条熄灭.
(4)取12g石灰石样品放入盛有105.4g稀盐酸溶液的烧杯中,恰好完全反应.有关实验数据如下表:(假设石灰石样品中杂质不与稀盐酸反应也不溶于水,且不考虑反应过程中水分和HCl气体的挥发)
②反应中生成二氧化碳的质量为4.4g.
②该石灰石样品中碳酸钙的质量分数为83.3%(结果精确到0.1%).
 某化学兴趣小组的同学设计了如下实验来验证二氧化碳气体的相关性质,实验步骤如下:
某化学兴趣小组的同学设计了如下实验来验证二氧化碳气体的相关性质,实验步骤如下:Ⅰ.取一个三通管(三个管口都未密封,与空气相通),在三通管的上部和下部各放一张湿润的蓝色石蕊试纸(湿润的蓝色石蕊试纸遇到酸性物质会变红).然后将它与二氧化碳的发生装置连接.(如图1,整套装置的气密性良好)
Ⅱ.打开分液漏斗的活塞,使石灰石与稀盐酸接触,观察到相关现象后,停止实验.
Ⅲ.取下图1中的三通管,把贴有试纸B的那端放在酒精灯火焰上加热(如图2),
观察实验现象.
注:整个实验中不考虑反应过程中水分和HCl气体的挥发,且图1中产生的气流较缓慢
根据上述实验,回答下列问题:
(1)实验Ⅱ步骤中三通管内产生的实验现象是b处湿润的蓝色湿润试纸变红;由此说明二氧化碳气体具有二氧化碳密度大于空气、二氧化碳能与水反应的性质.
(2)实验Ⅲ步骤中一定发生的化学反应方程式是H2CO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2↑;
(3)若不改变图1的实验装置,还要验证二氧化碳气体具有不能燃烧、也不能支持燃烧的性质,需要补充的实验是取一根燃着的小木条放在b导管口,发现小木条熄灭.
(4)取12g石灰石样品放入盛有105.4g稀盐酸溶液的烧杯中,恰好完全反应.有关实验数据如下表:(假设石灰石样品中杂质不与稀盐酸反应也不溶于水,且不考虑反应过程中水分和HCl气体的挥发)
| 反应前 | 反应后 | ||
| 实验 数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 150g | 12g | 157.6g | |
②该石灰石样品中碳酸钙的质量分数为83.3%(结果精确到0.1%).
11.要除去铁制品表面的铁锈,可以用下列哪种物质( )
| A. | 水 | B. | 食盐 | C. | 稀盐酸 | D. | 氢氧化钠溶液 |
8.用I2O5可以测定空气受CO污染的程度,发生反应的化学方程式如下:I2O5+5CO═I2+5X,关于这个反应X的化学式为( )
| A. | CO | B. | CO2 | C. | H2O | D. | O2 |
9.下列金属各2g,分别于足量稀盐酸反应,生成氢气最多的是( )
| A. | Al | B. | Mg | C. | Fe | D. | Zn |