题目内容
CaSO4和KH2PO4的混合物中,测得其中硫元素的质量分数约为11.8%,则混合物中氧元素的质量分数为
- A.23.6%
- B.45.8%
- C.47.1%
- D.无法确定
C
分析:根据完整中元素的质量分数= ×100%,进行解答.
×100%,进行解答.
解答:根据完整中元素的质量分数= ×100%,可得
×100%,可得
CaSO4中O的质量分数=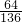 ×100%=47.1%
×100%=47.1%
KH2PO4中O的质量分数═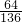 ×100%=47.1%
×100%=47.1%
由此可知无论两者比例如何,氧元素的质量分数都是47.1%;
故选C.
点评:本题考查学生对等量法的理解与掌握,并能在解题中灵活应用的能力.
分析:根据完整中元素的质量分数=
 ×100%,进行解答.
×100%,进行解答.解答:根据完整中元素的质量分数=
 ×100%,可得
×100%,可得CaSO4中O的质量分数=
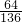 ×100%=47.1%
×100%=47.1%KH2PO4中O的质量分数═
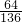 ×100%=47.1%
×100%=47.1%由此可知无论两者比例如何,氧元素的质量分数都是47.1%;
故选C.
点评:本题考查学生对等量法的理解与掌握,并能在解题中灵活应用的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
CaSO4和KH2PO4的混合物中,测得其中硫元素的质量分数约为11.8%,则混合物中氧元素的质量分数为( )
| A、23.6% | B、45.8% | C、47.1% | D、无法确定 |