题目内容
1.下列推理正确的是( )| A. | 酸碱中和反应生成盐和水,则生成盐和水的反应一定是中和反应 | |
| B. | CO2能灭火,能使燃着的木条熄灭的无色气体不一定是CO2 | |
| C. | 金属和酸反应能生成气体,和酸反应生成气体的物质一定是金属 | |
| D. | 某有机物燃烧生成CO2和H2O,该有机物中一定含有C、H、O三种元素 |
分析 A、根据中和反应是酸与碱作用生成盐和水的反应解答;
B、根据二氧化碳的性质进行解答;
C、根据碳酸盐也可以和酸反应生成气体进行解答;
D、根据质量守恒定律进行解答.
解答 解:
A、酸碱中和反应能生成盐和水,生成盐和水的反应不一定是中和反应,如CO2+2NaOH═Na2CO3+H2O,故选项说法错误.
B、CO2能灭火,能使燃着的木条熄灭的无色气体不一定是CO2,例如氮气也能使燃着的木条熄灭,故B正确;
C、碳酸盐也可以和酸反应生成气体,所以和酸反应生成气体的物质不一定是金属,故C错误;
D、某有机物燃烧生成CO2和H2O,该有机物中一定含有C、H,但不一定含有氧元素,故D错误.
故选:B.
点评 本题难度不大,掌握中和反应的特征、物质的元素组成等即可正确解答本题.了解物质的构成以及常见物质的性质和质量守恒定律,属于基础知识.

练习册系列答案
相关题目
12.甲同学欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”之一命题.该同学设计并完成了下表所示的探究实验:
(1)请你帮甲同学填写上表中未填完的空格;
(2)在甲的探究实验中,实验一和实验二起的作用是对比;
(3)乙同学认为仅由上述实验还不能完全得出表内“总结”,乙同学补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明.
第一方面的实验操作中包含了两次称量,其目的是:比较MnO2在过氧化氢分解前后的质量;
第二方面的实验是利用“实验三”反应后试管内的剩余物继续实验.接下来的实验操作、现象和结论是:向剩余的固体中重新加人过氧化氢溶液,伸入带火星的木条,有大量气泡产生,木条复燃,说明MnO2仍然能加快过氧化氢的分解..
| 实验操作 | 实验现象 | 实验结论或总结 | ||
| 结论 | 总结 | |||
| 实验一 | 取5mL 5%的过氧化氢溶液于试管中,伸入带火星的木条 | 有气泡产生,木条不复燃 | 过氧化氢分解产生氧气,但是反应慢.反应的化学方程式为2H2O2=2H2O+O2↑ | 二氧化锰是过氧化氢分解的催化剂 |
| 实验二 | 向盛水的试管中加入二氧化锰,伸入带火星的木条 | 没有明显现象 | 二氧化锰加入水中不产生氧气 | |
| 实验三 | 向盛有5mL5%的过氧化氢溶液的试管中加入二氧化锰,伸入带火星的木条 | 大量气泡产生,带火星的木条迅速复燃 | 二氧化锰能加快过氧化氢的分解 | |
(2)在甲的探究实验中,实验一和实验二起的作用是对比;
(3)乙同学认为仅由上述实验还不能完全得出表内“总结”,乙同学补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明.
第一方面的实验操作中包含了两次称量,其目的是:比较MnO2在过氧化氢分解前后的质量;
第二方面的实验是利用“实验三”反应后试管内的剩余物继续实验.接下来的实验操作、现象和结论是:向剩余的固体中重新加人过氧化氢溶液,伸入带火星的木条,有大量气泡产生,木条复燃,说明MnO2仍然能加快过氧化氢的分解..
9.在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化见下表,下列说法中不正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前物质质量/g | 8 | 32 | 5 | 4 |
| 反应后物质质量/g | 16 | 4 | x | 24 |
| A. | 该反应为分解反应 | |
| B. | 丙可能为该反应的催化剂 | |
| C. | 该反应中甲、乙两种物质间的质量比为1:4 | |
| D. | 乙中含有两种或两种以上元素 |
13.下列四个图象中,能正确反映对应变化关系的是( )
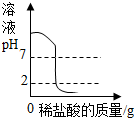 | 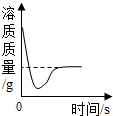 | 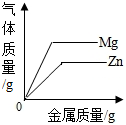 | 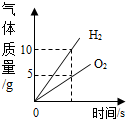 |
| A.向一定量的氢氧化钠溶液中逐滴加入pH=2的稀盐酸至过量 | B.某温度时,向一定量的饱和石灰水中加入少量生石灰 | C.向两份完全相同的稀盐酸中分别加入足量的锌粉、镁粉 | D.将水通电一段时间 |
| A. | A | B. | B | C. | C | D. | D |
