题目内容
11.不锈钢耐腐蚀性比较强,做为主要添加元素之一的锰元素(Mn)起着重要的作用.某同学为了探究锰、镁、铜三种金属的活动性,进行了如下实验:
①用砂纸对锰片进行打磨;
②将一小片锰片放入到硫酸镁溶液中,一段时间后,锰片表面无明显变化;
③将一小锰片放入到硫酸铜溶液中,一段时间后,锰片表面有红色物质生成.
请回答:(1)砂纸打磨锰片的目的是去除表面氧化物;
(2)三种金属的活动性由强到弱的顺序是镁>锰>铜(或Mg>Mn>Cu);
(3)步骤③中反应的化学方程式为Mn+CuSO4=Cu+MnSO4(锰在该化合物中显+2价).
分析 (1)根据砂纸打磨锰片的目的是去除表面氧化物解答;
(2)根据“活动性较强的金属一般可以将位于其后的金属从它们的盐溶液中置换出来”分析解答;
(3)根据“活动性较强的金属一般可以将位于其后的金属从它们的盐溶液中置换出来”分析解答.
解答 解:
(1)砂纸打磨锰片的目的是去除表面氧化物;
(2)活动性较强的金属一般可以将位于其后的金属从它们的盐溶液中置换出来.将锰片插入到氯化镁溶液中,一段时间后观察到锰片表面无明显变化,说明锰不能置换出镁,镁的活动性要比锰强;将锰片插入到氯化铜溶液中,一段时间后观察到锰片表面有红色物质生成,说明有可以置换出氯化铜溶液中的铜,锰的活动性比铜强.
所以三种金属的活动性由强到弱的顺序是:Mg>Mn>Cu.
故答案为:Mg>Mn>Cu.
(3)因为活动性较强的金属一般可以将位于其后的金属从它们的盐溶液中置换出来,所以单质锰(Mn)与氯化铜溶液反应,可以把铜置换出来.
故答案为:Mn+CuCl2═MnCl2+Cu.
答案:
(1)去除表面氧化物;
(2)镁>锰>铜(或Mg>Mn>Cu);
(3)Mn+CuSO4=Cu+MnSO4
点评 本题考查铁生锈的条件、材料的组成、金属的活动性顺序,属于对基础知识的运用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.逻辑推理是化学学习中常用的思维方法.以下推理正确的是( )
| A. | 有机物是含有碳元素的化合物,因此,含有碳元素的化合物都是有机物 | |
| B. | 氧化物是含有氧元素的化合物,所以,含有氧元素的化合物都是氧化物 | |
| C. | 中和反应生成盐和水,因此,生成盐和水的反应都是中和反应 | |
| D. | CO2气体能使燃烧的木条熄灭,但能使燃烧的木条熄灭的气体不一定是CO2 |
3.在一定条件下,发生如下转化关系:甲+乙→丙+丁,下列说法正确的是( )
| A. | 若乙为O2、丙为CO2、丁为H2O,则甲一定是蜡烛 | |
| B. | 若丙为盐、丁为水,则甲和乙的反应一定是酸碱中和反应 | |
| C. | 若甲、丙为金属单质,乙、丁为盐,则甲的金属活动性一定比丙强 | |
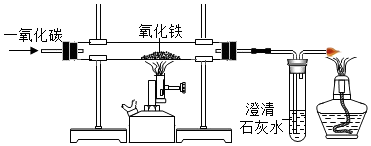
| D. | 若乙为CO、丙为Fe、丁为CO2,则甲一定是Fe2O3 |
20.下列方程是符合题意书写且基本反应类型均正确的是( )
| A. | 加熟石灰研磨,检验铵态氮肥 NH4NO3+Ca(OH)2═CaNO3+NH3↑+H2O 复分解反应 | |
| B. | 煅烧石灰石制生石灰 CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ 分解反应 | |
| C. | 碳酸根离子的检验 Na2CO3+Ca(OH)2═CaCO3↓+2NaOH 复分解反应 | |
| D. | 用氢氧化铝治疗胃酸过多 3H2SO4+2Al(OH)3═Al2(SO4)3+3H2O 中和反应 |