题目内容
9. 某化学兴趣小组的同学们欲测定一定量的某种石灰石样品中碳酸钙的质量,进行了如下实验:
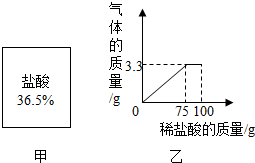
某化学兴趣小组的同学们欲测定一定量的某种石灰石样品中碳酸钙的质量,进行了如下实验:(1)配制100g溶质质量分数为7.3%的稀盐酸,需图甲所示盐酸的质量为20g.
(2)将(1)中配制好的稀盐酸加人盛有石灰石样品的烧杯中,产生气体的质量与加入稀盐
酸的质量关系如图乙所示(假设石灰石样品中的杂质不与稀盐酸反应).
计算:该石灰石样品中碳酸钙的质量.
分析 (1)根据稀释前后溶质的质量不变进行分析;
(2)根据题中所给的数据和化学方程式进行分析即可.
解答 解:(1)用这瓶浓盐酸来配制100g溶质质量分数为7.3%的稀盐酸,需量取这种浓盐酸的质量是:$\frac{100g×7.3%}{36.5%}$=20g;
(2)设参加反应的碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73
x 75g×7.3%
$\frac{100}{x}$=$\frac{73}{75g×7.3%}$
x=7.5g
所以该石灰石中碳酸钙的质量为7.5g.
故答案为:(1)20;
(2)该石灰石中碳酸钙的质量为7.5g.
点评 本题主要考查了溶质的质量分数的相关计算和依据化学方程式的计算,难度不大,但解答时要细心计算.

练习册系列答案
相关题目
17.如表是不同温度时NaCl、KNO3的溶解度.则下列说法正确的是( )
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | |
| A. | 将60℃时KNO3的饱和溶液降温至20℃,溶质、溶剂的质量都会减少 | |
| B. | 40℃时,将50g NaCl、50g KNO3分别加入100g水中,所得溶液的溶质质量分数不相等 | |
| C. | 将80℃时NaCl、KNO3两种饱和溶液降温至20℃,析出晶体的质量一定是KNO3>NaCl | |
| D. | 用上表数据绘制成NaCl、KNO3的溶解度曲线,两条曲线交点对应的温度范围是0~20℃ |
14.下列物质属于纯净物的是( )
| A. | 盐水 | B. | 雨水 | C. | 冰水 | D. | 海水 |
1.甲乙丙丁四种物质的转化关系如图所示.下列说法正确的是( )
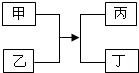

| A. | 若甲、丁为单质,则该反应一定是置换反应 | |
| B. | 若丙为气体,则甲、乙中一定有单质 | |
| C. | 若丙为沉淀,则甲、乙中一定有一种物质是碱 | |
| D. | 若丁为水,则该反应一定是复分解反应 |
2.下列化学用语与含义相符的是( )
| A. | H2--氢分子 | B. | 2O--2个氧元素 | C. | Na2+--钠离子 | D. | CO--一氧化碳 |
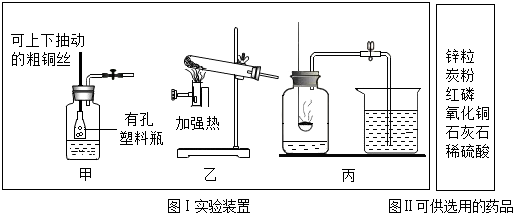
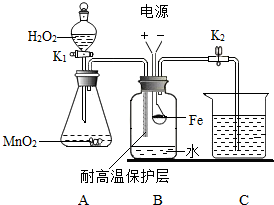 某同学用图14所示装置研究铁丝燃烧实验.
某同学用图14所示装置研究铁丝燃烧实验.