题目内容
3.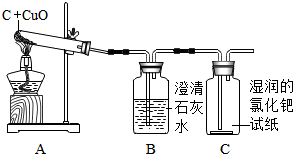 李洋同学在实验室用木炭和氧化铜两种黑色粉末在高温下反应制取单质铜,反应的化学方程式为:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ 他联想到单质碳的一些化学性质,认为在该实验中还可能会有CO产生.
李洋同学在实验室用木炭和氧化铜两种黑色粉末在高温下反应制取单质铜,反应的化学方程式为:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ 他联想到单质碳的一些化学性质,认为在该实验中还可能会有CO产生.查阅资料:CO气体能使湿润的黄色氯化钯试纸变蓝色.
实验验证:
(1)点燃A处酒精灯,数分钟后发现试管中的黑色固体物质变红,该红色物质是铜;
(2)装置B的作用是检验A装置反应是否发生;
(3)C装置中湿润的黄色氯化钯试纸变蓝色,说明有CO气体生成,证明李洋同学的判断正确.
实验反思:
(4)李洋同学对CO产生的原因进行了分析:
①原因一:木炭和氧化铜在高温条件下直接发生反应产生CO;
②原因二:反应C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑中的一种产物和反应物木炭又发生了新的化学反应,产生了CO;
③原因三:不用填
如果是原因一反应的化学方程式是C+CuO$\frac{\underline{\;高温\;}}{\;}$Cu+CO↑;
如果是原因二,反应的化学方程式是CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
(5)从环保角度考虑,你认为该装置还需要做怎样的改进尾气处理或点燃尾气或尾气收集.
分析 (1)试管中发生反应C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑,则黑色的氧化铜变为红色的铜;
(2)二氧化碳能与澄清石灰水反应,使澄清石灰水变浑浊.可检验气体中含有二氧化碳;
(3)因为CO气体能使湿润的黄色氯化钯试纸变蓝色,可用湿润的氯化钾试纸变色检验产生了一氧化碳气体;
(4)注意反应的顺序,要注意对化学方程式进行配平;
(5)一氧化碳是有毒气体,对大气有污染,因此要对一氧化碳进行吸收或处理后再排放.
解答 解:(1)试管中发生反应C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑,产生红色的铜;
(2)二氧化碳使澄清石灰水变浑浊,以此检验是否有二氧化碳气体产生;
(3)可用湿润的氯化钾试纸变色检验产生了一氧化碳气体;
(4)CuO+C$\frac{\underline{\;高温\;}}{\;}$Cu+CO↑,CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;
(5)因为一氧化碳为有毒气体,需进行处理,则在C装置后面增加一个尾气处理装置,如放置一只点燃的酒精灯或套上一只气球等.
故答案为:(1)铜;
(2)检验A装置反应是否发生;
(3)CO;
(4)C+CuO$\frac{\underline{\;高温\;}}{\;}$Cu+CO↑或CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;
(5)尾气处理或点燃尾气或尾气收集.
点评 本实验侧重考查学生的观察与思考能力,对碳以及碳的氧化物一些性质及一些产常见的变色反应进行了考查.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.对于天宫一号目标飞行器内镍氢电池的总反应式H2+2NiO(OH)═2Ni(OH)2,下列叙述不正确的是( )
| A. | 该反应是化合反应 | |
| B. | 参加反应的H2与NiO(OH)的质量比为1:92 | |
| C. | NiO(OH)是氧化物 | |
| D. | Ni(OH)2中Ni化合价为+2价 |
5.下列有关说法正确的是( )
| A. | 火灾发生后应用湿毛巾捂住口鼻迅速逃离,并拨打火警119 | |
| B. | 煤、石油、天然气属于可再生资源,取之不尽、用之不竭 | |
| C. | 只要达到着火点,可燃物一定会燃烧 | |
| D. | 可燃物燃烧的同时一定还会发生爆炸 |
2.测定人体内体液的pH可以帮助我们了解身体状况,如图是明明同学体检报告单截图,看图后回答问题.
(1)该同学哪项指标出现异常胃液pH偏小.
(2)医生让明明服用一种主要成分为氢氧化铝的药物,请写出该反应的化学方程式Al(OH)3+3HCl=AlCl3+3H2O.
(3)一些食物的近似pH如下:①番茄4.0-4.4②苹果2.9-3.3③牛奶6.3-6.6④鸡蛋清7.6-8.0,明明适宜的食物是④(填序号).
| 项目 | 检测值 | 正常pH范围 |
| 血浆 | 7.41 | 7.35-7.45 |
| 胃液 | 0.8 | 0.9-1.5 |
| 胆汁 | 7.21 | 7.1-7.3 |
| 胰液 | 7.8 | 7.5-8.0 |
(2)医生让明明服用一种主要成分为氢氧化铝的药物,请写出该反应的化学方程式Al(OH)3+3HCl=AlCl3+3H2O.
(3)一些食物的近似pH如下:①番茄4.0-4.4②苹果2.9-3.3③牛奶6.3-6.6④鸡蛋清7.6-8.0,明明适宜的食物是④(填序号).
8.以下是初中化学中的一些基本实验,不能达到实验目的是( )
| A. | 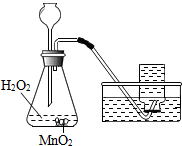 制取氧气 | B. | 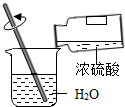 稀释浓硫酸 | ||
| C. | 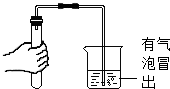 检查装置气密性 | D. | 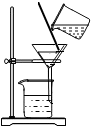 粗盐过滤 |
15.下列物质中,主要成分不同的一组是( )
| A. | 沼气和天然气 | B. | 酒精和乙醇 | C. | 生石灰和氧化钙 | D. | 干冰和冰 |
13.下列物质的应用不正确的是( )
| A. |  钛合金制成人造骨 | B. |  氢氧化钠制叶脉书签 | ||
| C. |  炉具清洁剂清洗餐具 | D. |  增加水中的含氧量 |