题目内容
为测定某CuSO4溶液的溶质质量分数,化学小组的同学取CuSO4溶液100g,向其中滴加一定浓度的NaOH溶液,至不再产生沉淀为止,共用去NaOH溶液80g,过滤,得到滤液175.1g.请计算:
(1)该反应生成沉淀 4g;
(2)该CuSO4溶液中溶质的质量分数.
(温馨提示:CuSO4+2NaOH═Cu(OH)2↓+Na2SO4)
| 根据化学反应方程式的计算;有关溶质质量分数的简单计算. | |
| 专题: | 溶质质量分数与化学方程式相结合的计算. |
| 分析: | (1)根据质量守恒定律求出沉淀的质量; (2)根据化学反应方程式列式计算,根据生成Cu(OH)2沉淀的质量可求出参加反应的CuSO4质量,进而可求出CuSO4溶液中溶质的质量分数; |
| 解答: | 解: (1)反应生成沉淀的质量为100g+80g﹣175.1g=4.9g (2)设100g CuSO4溶液中所含CuSO4质量为x CuSO4+2NaOH═Na2SO4+Cu(OH)2↓ 160 98 x 4.9g
x=8g CuSO4溶液中溶质的质量分数= 答案: (1)4.9 (2)CuSO4溶液中溶质的质量分数为8% |
| 点评: | 本题考查学生利用化学反应方程式来进行的有关计算,学生应明确物质能否反应,发生的什么反应,熟悉常见的化学反应是解答此类习题的关键. |

X,Y,Z三种物质的溶解度曲找如图所示.将t2℃时三种物质的饱和溶液降温至t1℃,溶液中溶质的质量分数的大小关系正确的是( )

|
| A. | X>Y>Z | B. | Y>Z>X | C. | Z>Y>X | D. | X=Y>Z |
酚酞(C20H14O4)是实验室常用的指示剂.下列说法不正确的是( )
|
| A. | 酚酞是有机物 |
|
| B. | 酚酞由碳、氢、氧三种元素组成 |
|
| C. | 酚酞的相对分子量为318 |
|
| D. | 酚酞中碳、氢、氧元素的质量比为20:14:4 |
维生素对调节人体新陈代谢、维持身体健康有重要作用,下列食物中富含维生素的是( )
|
| A. | 奶油 | B. | 蔬菜 | C. | 小麦粉 | D. | 白砂糖 |
同学们填写的“毕业生登记表”需要长期保存,因此书写时必须使用( )
|
| A. | 铅笔 | B. | 圆珠笔 | C. | 红墨水笔 | D. | 碳素笔 |
认识燃烧原理可以利用和控制燃烧,下列说法正确的是( )
|
| A. | 物质与氧气反应时都会发生燃烧 |
|
| B. | 只要达到燃烧所需的最低温度,可燃物就能燃烧 |
|
| C. | 把木柴架空,可使木柴更充分接触空气而燃烧得更旺 |
|
| D. | 用嘴吹蜡烛,蜡烛熄灭是因为降低了蜡烛的着火点 |
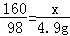
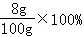 =8%
=8%
