题目内容
8.写出下列物质的名称或化学符号:(1)NaCl氯化钠;
(2)2H+两个氢离子;
(3)2O2两个氧分子;
(4)氯化铁FeCl3 ;
(5)4个氢氧根离子4OH-;
(6)氦气He;
(7)水银Hg.
分析 本题考查物质的化学式及名称的基本书写.根据化学式的读法,及物质的构成可以作答.
解答 (1)化学式的读法从右向左,故名称为氯化钠;(2)离子前面的数字表示离子的个数,故名称为两个氢离子;(3)分子前面的数字表示分子个数,故名称为两个氧分子;(4)氯化铁中铁元素显正三价,根据正价在左,负价在右,可以写出化学式为FeCl3;(5)氢氧根离子是原子团,为OH-,四个氢氧根离子,个数写在符号的前面,故答案为4OH-;(6)氦气是由原子构成的,所以用元素符号可以代表氦气这种物质,故答案为He;(7)水银也是由原子构成的,故答案为Hg.
(1)氯化钠(2)两个氢离子(3)两个氧分子(4)FeCl3 (5)4OH- (6)He (7)Hg
点评 本题比较简单,是基础题目,易掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.某小组对H2O2溶液制氧气进行了如下探究:
(1)实验室用H2O2溶液和MnO2制取O2的反应符号表达式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,属于分解反应(填基本反应类型).
【探究一】:探究催化剂对H2O2分解速率的影响(实验中催化剂均为0.4g,H2O2浓度均为10%,以收集10mL气体为准)该小组采用了如图所示装置进行实验,具体数据如下表:
(2)写出有标号仪器的名称:①分液漏斗;②锥形瓶.
(3)检查A装置气密性的方法是夹住右侧导气管,打开①的两个活塞,向其中加水,若水不滴下(或漏斗下管口有水柱),则气密性良好.
(4)C装置应该选择C2,理由是反应放热,长导管可以将受放热影响排入量筒中的水回吸至B中减小实验误差.
(5)原装置中的空气对实验结果有没有影响?无;
(6)分析表格中数据,可以得出相同条件下表中催化剂的催化效果依次为活性炭>CuO>MnO2.
(7)为完成此探究,需要测定的数据有收集10mL氧气所需的时间.
【探究二】:探究H2O2溶液浓度对分解速率的影响(水浴温度控制在21℃,MnO2均为0.5g,H2O2溶液均为5mL,三颈瓶容积为250mL)
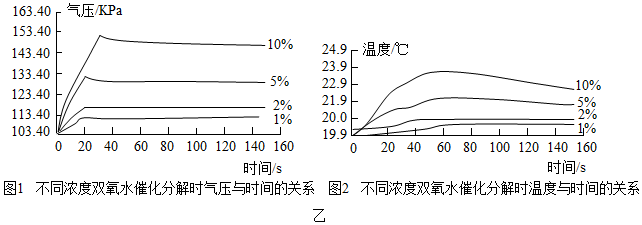
该小组采用了如图甲所示装置进行实验,并依据数字传感器数据绘制如图乙图象:

(8)实验中,恒压漏斗的作用是使H2O2溶液自行下滴(使漏斗及三颈瓶成为一个整体);
(9)图1说明H2O2溶液浓度越高,反应速率越快(填“快”或“慢”),以10%H2O2溶液为例,三颈瓶内气压由高缓慢降低的原因是反应结束,温度下降,气体也因冷却而收缩,使得三颈瓶内气压开始缓慢减小;
(10)图2说明从温度看,H2O2溶液浓度越高,反应越剧烈(填“剧烈”或“平稳”).
(1)实验室用H2O2溶液和MnO2制取O2的反应符号表达式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,属于分解反应(填基本反应类型).
【探究一】:探究催化剂对H2O2分解速率的影响(实验中催化剂均为0.4g,H2O2浓度均为10%,以收集10mL气体为准)该小组采用了如图所示装置进行实验,具体数据如下表:
| 催化剂种类 | 气体产生速率(mL/s) |
| MnO2 | 0.03 |
| CuO | 0.07 |
| 活性炭 | 0.12 |
(3)检查A装置气密性的方法是夹住右侧导气管,打开①的两个活塞,向其中加水,若水不滴下(或漏斗下管口有水柱),则气密性良好.
(4)C装置应该选择C2,理由是反应放热,长导管可以将受放热影响排入量筒中的水回吸至B中减小实验误差.
(5)原装置中的空气对实验结果有没有影响?无;
(6)分析表格中数据,可以得出相同条件下表中催化剂的催化效果依次为活性炭>CuO>MnO2.
(7)为完成此探究,需要测定的数据有收集10mL氧气所需的时间.
【探究二】:探究H2O2溶液浓度对分解速率的影响(水浴温度控制在21℃,MnO2均为0.5g,H2O2溶液均为5mL,三颈瓶容积为250mL)
该小组采用了如图甲所示装置进行实验,并依据数字传感器数据绘制如图乙图象:


(8)实验中,恒压漏斗的作用是使H2O2溶液自行下滴(使漏斗及三颈瓶成为一个整体);
(9)图1说明H2O2溶液浓度越高,反应速率越快(填“快”或“慢”),以10%H2O2溶液为例,三颈瓶内气压由高缓慢降低的原因是反应结束,温度下降,气体也因冷却而收缩,使得三颈瓶内气压开始缓慢减小;
(10)图2说明从温度看,H2O2溶液浓度越高,反应越剧烈(填“剧烈”或“平稳”).
3.如图为某反应的微观示意图,下列说法不正确的是( )


| A. | 反应后的物质是混合物 | |
| B. | 反应的AB与B2的分子个数比为2:3 | |
| C. | 该反应说明化学为化中分子可分 | |
| D. | 两种元素化合时,原子个数比不唯一 |
13.碘元素(符号为I)具有预防和治疗甲状腺肿的作用,人体缺碘时易患大脖子病.为了消除碘缺乏病,我国政府规定居民的食用盐必须是加碘盐,简称碘盐.所谓碘盐就是在食盐中加入碘酸钾.下表是江西省盐业公司专营的精制碘盐包装袋上的部分说明文字.请回答下列问题:
(1)已知碘酸钾的化学式为KIO3,试计算:
①碘酸钾中碘元素(I)的化合价.
②碘酸钾中碘元素的质量分数
(2)由食用方法和贮藏指南可以推测碘酸钾的性质之一是:受热易分解.
(3)若1000g碘盐中含20mg碘.
①这里标明的碘的含量是指B
A.碘单质 B.碘元素 C.碘原子 D.碘分子
②已知成人每天约需要0.15mg碘,假设这些碘主要是从碘盐中摄取的,则成人每天需要食用碘盐多少克?
| 配料表 | 食用盐、碘酸钾 |
| 含碘量 | (20mg~40mg)/kg |
| 保质期 | 18个月 |
| 食用方法 | 待食物烹调好后再放入碘盐,勿长时间炖炒 |
| 贮藏指南 | 避热、避光、密封、防潮 |
①碘酸钾中碘元素(I)的化合价.
②碘酸钾中碘元素的质量分数
(2)由食用方法和贮藏指南可以推测碘酸钾的性质之一是:受热易分解.
(3)若1000g碘盐中含20mg碘.
①这里标明的碘的含量是指B
A.碘单质 B.碘元素 C.碘原子 D.碘分子
②已知成人每天约需要0.15mg碘,假设这些碘主要是从碘盐中摄取的,则成人每天需要食用碘盐多少克?
17.下列物质的分类不正确的是( )
| A. | 混合物:空气、臭氧、海水 | B. | 氧化物:水、二氧化碳、五氧化二磷 | ||
| C. | 化合物:氧化铁、二氧化锰、锰酸钾 | D. | 单质:铁、氧气、硫 |
 某化学课外小组的同学,在实验室实验时发现一瓶标签破损的无色溶液(如图所示).
某化学课外小组的同学,在实验室实验时发现一瓶标签破损的无色溶液(如图所示).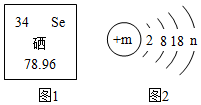 如图1是元素周期表中的一部分,图2是硒原子的结构示意图.据图回答问题:
如图1是元素周期表中的一部分,图2是硒原子的结构示意图.据图回答问题: