题目内容
5.请回答家庭生活中的问题:(1)熄灭生日蜡烛时都用吹灭的方法,其原理是降低温度到着火点以下.
(2)某些地区的家庭使用的燃料是天然气,它燃烧的方程式为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(3)某些食品包装中有一小袋干燥剂(成分为生石灰),生石灰可用作干燥剂的原因是CaO+H2O═Ca(OH)2;若将其投入水中并滴入紫色石蕊试液,溶液变蓝色.
(4)将未喝完的碳酸饮料放在教室的窗台上,阳光晒过之后,发现瓶内壁上有大量气泡,产生气泡的原因是碳酸分解生成二氧化碳气体.
分析 (1)要根据灭火的原理考虑:隔绝空气、降低温度到可燃物的着火点以下、移走可燃物;
(2)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可;
(3)生石灰能与水反应生成氢氧化钙,结合石蕊溶液遇酸性溶液变红色,遇碱性溶液变蓝色,进行分析解答;
(4)碳酸受热容易分解生成水和二氧化碳.
解答 解:(1)吹蜡烛时,气流带走了大量的热,使石蜡的温度降到了着火点以下,因此蜡烛熄灭;
(2)天然气的主要成分是甲烷,甲烷在点燃条件下燃烧生成二氧化碳和水,反应的化学方程式为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(3)生石灰与水反应生成氢氧化钙,吸收水蒸汽的化学方程式为:CaO+H2O═Ca(OH)2.
将其投入水中,生成的氢氧化钙溶液具有碱性,滴入紫色石蕊试液,溶液变蓝色.
(4)将未喝完的碳酸饮料放在教室的窗台上,阳光晒过后,发现瓶的内壁上有大量气泡,产生气泡的原因是碳酸受热分解生成了二氧化碳气体.
故答案为:(1)降低温度到着火点以下.
(2)CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(3)CaO+H2O═Ca(OH)2;蓝.
(4)碳酸分解生成二氧化碳气体.
点评 本题考查灭火的方法、化学方程式的书写等基础知识.知识点较多,但难度不大.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案
相关题目
15.重铬酸钾(K2Cr2O7)可用于测定酒驾中的酒精(C2H5OH)含量.下列说法正确的是( )
| A. | K2Cr2O7中铬元素的化合价为+7 | |
| B. | K2Cr2O7属于氧化物 | |
| C. | C2H5OH中碳、氢、氧三种元素的质量比为12:3:8 | |
| D. | C2H5OH中C、H、O的原子个数比为2:5:1 |
13.乙醇(C2H5OH)完全燃烧时生成CO2和H2O,如果氧气不充分,乙醇燃烧后可能还有CO生成.现用以下装置进行实验,确证乙醇燃烧产物中有CO、CO2和H2O.
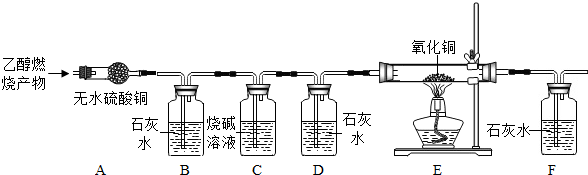
(1)实验时,可以观察到装置B、F石灰水都变浑浊,D中石灰水不变浑浊.F装置的作用是证明乙醇燃烧产物中是否有CO.
(2)若乙醇在氧气中不充分燃烧时的化学方程式可以表示为:xC2H5OH+yO2═aCO2+bCO+cH2O;现有
一定质量的乙醇燃烧时,得到了4.4g二氧化碳和1.4g一氧化碳,则符合此反应的化学方程式中a和b的比值为2:1.
(3)上述装置化学反应中通常伴随有能量的变化,可借助反应前后的温度变化来判断反应的发生.如NaOH溶液与稀盐酸混合前后温度有变化,则证明发生了化学反应.该组同学将不同溶质质量分数的盐酸和NaOH溶液各10mL混合,用温度计测定室温下混合前后温度的变化,并记录了每次混合前后温度的升高值△t(如下表).
①表中x=7.
②某同学在没使用温度计的情况下,通过如图所示装置也可以判断NaOH溶液与稀盐酸发生了反应,该同学判断依据是U形管中液面左低右高(不考虑烧瓶内液体体积的变化对实验的影响).

(1)实验时,可以观察到装置B、F石灰水都变浑浊,D中石灰水不变浑浊.F装置的作用是证明乙醇燃烧产物中是否有CO.
(2)若乙醇在氧气中不充分燃烧时的化学方程式可以表示为:xC2H5OH+yO2═aCO2+bCO+cH2O;现有
一定质量的乙醇燃烧时,得到了4.4g二氧化碳和1.4g一氧化碳,则符合此反应的化学方程式中a和b的比值为2:1.
(3)上述装置化学反应中通常伴随有能量的变化,可借助反应前后的温度变化来判断反应的发生.如NaOH溶液与稀盐酸混合前后温度有变化,则证明发生了化学反应.该组同学将不同溶质质量分数的盐酸和NaOH溶液各10mL混合,用温度计测定室温下混合前后温度的变化,并记录了每次混合前后温度的升高值△t(如下表).
| 编号 | 盐酸 | NaOH溶液 | △t/℃ | 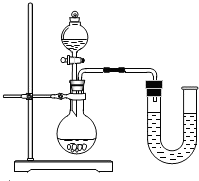 |
| 1 | 3.65% | 2.00% | 3.5 | |
| 2 | 3.65% | 4.00% | x | |
| 3 | 7.30% | 8.00% | 14 |
②某同学在没使用温度计的情况下,通过如图所示装置也可以判断NaOH溶液与稀盐酸发生了反应,该同学判断依据是U形管中液面左低右高(不考虑烧瓶内液体体积的变化对实验的影响).
20.下列反应属于中和反应的是( )
| A. | CaO+2HCl═CaCl2+H2O | B. | HCl+KOH═KCl+H2O | ||
| C. | 2NaOH+CuSO4═Cu(OH)2↓+Na2SO4 | D. | Ca(OH)2+CO2═CaCO3↓+H2O |
17.某物质在氧气中完全燃烧生成8.8g二氧化碳和5.4g水,则关于该物质的组成描述正确的是( )
| A. | 该物质一定含有碳元素和氢元素,可能含有氧元素 | |
| B. | 该物质中碳元素与氢元素的质量比为12:1 | |
| C. | 该物质只含有碳元素和氢元素 | |
| D. | 该物质的分子中碳原子和氢原子的个数比为1:2 |
14.下列日常生活中的现象,属于物理变化的是( )
| A. | 食物腐烂 | B. | 钢铁生锈 | C. | 天然气燃烧 | D. | 盐酸挥发 |
8.如图所示的实验操作正确的是( )
| A. |  闻气味 | B. | 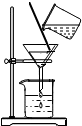 过滤液体 | ||
| C. | 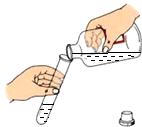 倾倒液体 | D. | 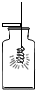 铁丝在氧气中燃烧 |
