题目内容
20.除去下列各物质中混有的少量杂质,所用试剂和操作均正确的是( )| 序号 | 物质 | 杂质 | 所用试剂和操作方法 |
| A | Na2CO3溶液 | Na2SO4溶液 | 加入过量的Ba(NO3)2溶液,过滤 |
| B | H2 | HCl | 通过足量的NaOH溶液,浓硫酸 |
| C | NaCl固体 | 细沙 | 加入足量的水溶解、过滤 |
| D | 铁粉 | Fe2O3 | 加入适量的稀盐酸,过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、Na2CO3溶液和Na2SO4溶液均能与过量的Ba(NO3)2溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
B、HCl能与氢氧化钠溶液反应生成氯化钠和水,氢气不与氢氧化钠溶液反应,再通过浓硫酸进行干燥,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
C、氯化钠易溶于水,细沙难溶于水,可采取加水溶解、过滤、蒸发的方法进行分离除杂,故选项所采取的方法错误.
D、Fe2O3和铁粉均能与稀盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
故选:B.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案
相关题目
10.类推是学习化学的一种重要方法,但不恰当的类推又可能得出错误结论.以下类推正确的是( )
| A. | 原子和分子均是微观粒子,在化学变化中原子不能再分,则分子也不能再分 | |
| B. | 碱能跟非金属氧化物反应,则碱溶液一定能吸收二氧化碳、二氧化硫和一氧化碳气体 | |
| C. | 中和反应是酸和碱作用生成盐和水,则生成盐和水的反应不一定是中和反应 | |
| D. | 碳酸盐能与酸反应产生CO2,则与酸反应产生CO2的物质中一定含有CO32- |
15.某同学设计了以下四个实验方案,理论上正确,操作上可行,经济上合理的是( )
| A. | Cu$\stackrel{稀盐酸}{→}$CuCl2$\stackrel{NaOH溶液}{→}$Cu(OH)2 | |
| B. | H2O$\stackrel{通电}{→}$O2$\stackrel{Mg}{→}$MgO | |
| C. | CaCO3$\stackrel{高温}{→}$CaO$\stackrel{H_{2}O}{→}$Ca(OH)2$\stackrel{Na_{2}CO_{3}}{→}$NaOH溶液 | |
| D. | MgCl2$\stackrel{NaOH溶液}{→}$Mg(OH)2$\stackrel{Na}{→}$Mg |
5.实验室开放日,化学小组的同学来到实验室,对酸的性质很感兴趣,向老师提出研究硝酸的性质,老师高兴答应并带领同学们进行了硝酸性质的实验探究.
【实验设计】
(1)将石蕊试液滴入稀硝酸中,预计石蕊试液由紫色变红色;
(2)将Zn片投入稀硝酸中,预计将产生氢气.
【实验验证】同学们按上述设计做了实验,却发现石蕊变色后一会儿即褪去,Zn片投入稀HNO3后,溶液中冒出气泡,产生无色气体A,在试管口气体A变成红棕色有刺激性气味的气体B.
【提出问题】
(1)石蕊试液变色后为何会褪色?
(2)上述产生的无色气体是什么?硝酸具有哪些特性?
【查阅资料】看到如此异常的现象,在老师的指导下,同学们上网查到了下列资料:
(1)硝酸可与Zn、Cu等多种金属反应生成相应的硝酸盐,但不生成H2.
(2)含氮元素的某些气态物质的物理性质
【猜想与分析】
(1)小明同学认为石蕊变色后又褪色的原因是由于试管不干净,含有其他杂质造成的,要证明小明的观点,应进行的操作是取少量稀HNO3于干净的试管中,滴入石蕊试液.观察实验现象(或用干净的试管重复上述实验)
(2)大家一致认同了红棕色气体B是NO2,但对于无色气体A及变化的原因有不同的看法:
①小丽同学认为A是NH3,但遭到了大家的一致反对,原因是NH3极易溶于水,大多数气体会溶解在稀HNO3中.且在常温下NH3不易被氧化成NO2;
②小强同学认为A的N2,也遭到大家的一致反对,原因是N2的化学性质比较稳定,常温下,N2在空气中不能氧化成NO2;
③经讨论,最终大家获得了A是NO,NO在试管口遇氧气生成NO2的共识.
【实验探究】小红同学对硝酸与Cu反应很感兴趣,便取了一小块Cu片投入稀HNO3中,发现Cu片溶解,也出现了上述Zn与稀HNO3反应的类似现象,确认生成了NO,并在老师的帮助下,测出恰好反应的Cu和HNO3的质量比为8:21,由此获得了Cu与稀HNO3的反应化学方程式3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O.
【交流与反思】根据探究结果,请你解释稀HCl跟Cu不反应而稀HNO3却能跟Cu反应的原因铜不与稀HCl发生置换反应,是因为铜的金属活动性弱于氢.而稀HNO3具有强的氧化性,能与Cu发生氧化还原反应,生成NO等物质.
【实验设计】
(1)将石蕊试液滴入稀硝酸中,预计石蕊试液由紫色变红色;
(2)将Zn片投入稀硝酸中,预计将产生氢气.
【实验验证】同学们按上述设计做了实验,却发现石蕊变色后一会儿即褪去,Zn片投入稀HNO3后,溶液中冒出气泡,产生无色气体A,在试管口气体A变成红棕色有刺激性气味的气体B.
【提出问题】
(1)石蕊试液变色后为何会褪色?
(2)上述产生的无色气体是什么?硝酸具有哪些特性?
【查阅资料】看到如此异常的现象,在老师的指导下,同学们上网查到了下列资料:
(1)硝酸可与Zn、Cu等多种金属反应生成相应的硝酸盐,但不生成H2.
(2)含氮元素的某些气态物质的物理性质
| NH3 | N2 | NO | NO2 | |
| 颜色 | 无色 | 无色 | 无色 | 红棕色 |
| 溶解性 | 极易溶于水 | 不溶于水 | 不溶于水 | 可溶于水或硝酸 |
(1)小明同学认为石蕊变色后又褪色的原因是由于试管不干净,含有其他杂质造成的,要证明小明的观点,应进行的操作是取少量稀HNO3于干净的试管中,滴入石蕊试液.观察实验现象(或用干净的试管重复上述实验)
(2)大家一致认同了红棕色气体B是NO2,但对于无色气体A及变化的原因有不同的看法:
①小丽同学认为A是NH3,但遭到了大家的一致反对,原因是NH3极易溶于水,大多数气体会溶解在稀HNO3中.且在常温下NH3不易被氧化成NO2;
②小强同学认为A的N2,也遭到大家的一致反对,原因是N2的化学性质比较稳定,常温下,N2在空气中不能氧化成NO2;
③经讨论,最终大家获得了A是NO,NO在试管口遇氧气生成NO2的共识.
【实验探究】小红同学对硝酸与Cu反应很感兴趣,便取了一小块Cu片投入稀HNO3中,发现Cu片溶解,也出现了上述Zn与稀HNO3反应的类似现象,确认生成了NO,并在老师的帮助下,测出恰好反应的Cu和HNO3的质量比为8:21,由此获得了Cu与稀HNO3的反应化学方程式3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O.
【交流与反思】根据探究结果,请你解释稀HCl跟Cu不反应而稀HNO3却能跟Cu反应的原因铜不与稀HCl发生置换反应,是因为铜的金属活动性弱于氢.而稀HNO3具有强的氧化性,能与Cu发生氧化还原反应,生成NO等物质.
1.如图是甲、乙两位同学一起在实验室进行的氢氧化钠与盐酸中和反应的实验.(图中A1、A2、A3、B1、B2、B3均为溶液编号)
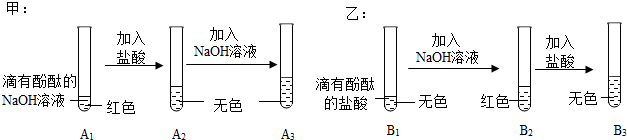
根据图中实验,请你与甲、乙同学一起完成下列探究:

根据图中实验,请你与甲、乙同学一起完成下列探究:
| 探究 环节 | 甲同学的探究 | 乙同学的探究 |
| 提出 问题 | A3溶液为什么不变红? | B3溶液中溶质成分是什么?(酚酞不计) |
| 做出 猜想 | 实验过程中,酚酞变质了? | 猜想一:NaCl 猜想二:NaCl HCl |
实验 验证 | (1)取少量A3溶液于另一试管中,向其中滴加NaOH溶液,溶液变红,说明甲同学的猜想不成立(填“成立”或“不成立”) (2)你认为在常温下A2溶液测出的pH <(填“>”、“=”或“<”)7 | 取少量B3溶液加入盛有少量铁粉的试管中,观察到有无色气泡产生,固体逐渐减少,溶液由无色变浅绿色,你认为乙同学的猜想二.(填“一”或“二”)成立 |
交流 反思 | (1)甲、乙同学的实验中,反应均涉及到的化学方程式是NaOH+HCl=NaCl+H2O. (2)A3溶液未变红,你认为原因是A2溶液中盐酸较多,加入的NaOH溶液未将其完全中和. (3)甲、乙同学经过实验对比探究,认为做化学实验时应注意药品用量的控制. | |

 我国古代将炉甘石(主要成分:ZnCO3)、赤铜矿(主要成分:Cu2O)和木炭粉为原料值得来黄铜(铜和锌的合金,外观似黄金),其生产流程如下:
我国古代将炉甘石(主要成分:ZnCO3)、赤铜矿(主要成分:Cu2O)和木炭粉为原料值得来黄铜(铜和锌的合金,外观似黄金),其生产流程如下: 化学就在我们身边.用我们学习的有关化学的概念和语言来填空.
化学就在我们身边.用我们学习的有关化学的概念和语言来填空.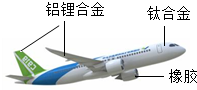 2015年11月,我国首架大型客机C919(如图)正式下线,实现了我国航空领域的新突破.回答下列问题:
2015年11月,我国首架大型客机C919(如图)正式下线,实现了我国航空领域的新突破.回答下列问题: