题目内容
5.实验室制取气体的装置如图:
(1)要制取纯净、干燥的CO2,写出装置中导管口从左到右的连接顺序.
(2)若选用A、E装置制取其他气体,写出有关反应的化学方程式.检验该气体是否收集满的操作方法是什么?
分析 (1)根据浓硫酸具有吸水性,碳酸氢钠溶液能吸收氯化氢气体等知识进行分析.
(2)考虑选用A、E装置制取氧气,考虑氧气的验满方法.
解答 解:
(1)先用碳酸氢钠溶液除去二氧化碳中混有的氯化氢气体,再用浓硫酸除去二氧化碳的水蒸气,最后用向上排空气法来收集,注意气体的长进短出.故要制取纯净、干燥的CO2,写出装置中导管口从左到右的连接顺序为a→g→f→e→d→h;
(2)若选用A、E装置制取其他气体,如氧气,反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;检验该气体是否收集满的操作方法是:将燃着的木条放到集气瓶口,若复燃,则集满.
故答案为:(1)a→g→f→e→d→h;
(2)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;将燃着的木条放到集气瓶口,若复燃,则集满.
点评 本题考查了常见气体的制取装置、收集方法等的选择及气体的性质,并在此基础上进行拓展,关键是明确发生装置、收集方法选择的依据.

练习册系列答案
相关题目
16.地壳中含量最多的元素是( )
| A. | 硅 | B. | 氧 | C. | 铝 | D. | 铁 |
13.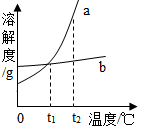 a、b两种物质的溶解度曲线如图所示,下列说法不正确的是( )
a、b两种物质的溶解度曲线如图所示,下列说法不正确的是( )
 a、b两种物质的溶解度曲线如图所示,下列说法不正确的是( )
a、b两种物质的溶解度曲线如图所示,下列说法不正确的是( )| A. | 将t1℃时b的饱和溶液加水可变为不饱和溶液 | |
| B. | 将t2℃时a的饱和溶液降温至t1℃,溶液质量减小 | |
| C. | t1℃时,两种物质的溶液溶质质量分数a=b | |
| D. | 将t2℃时a、b的饱和溶液分别降温至t1℃,两溶液的溶质质量分数相等 |
20.某同学利用如图装置验证二氧化碳的相关化学性质.
(1)步骤①中发生反应的化学方程式是Ca(OH)2+CO2=CaCO3↓+H2O.
(2)补全步骤②中的现象:紫色石蕊溶液变红.
(3)补全步骤③中的现象:溶液由红色变为蓝色,其中“气球1继续变大”的原因是二氧化碳与氢氧化钠反应使容器内气体减少,压强减小.
(4)通过本实验能验证的二氧化碳的化学性质是二氧化碳分别能与水、氢氧化钙、氢氧化钠反应.
| 实验装置 | 实验步骤 | 实验现象 |
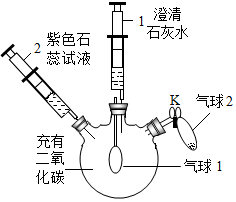 | ①向外拉注射器1 | 气球1微微鼓起, 注射器1中溶液变浑浊 |
| ②将注射器2中的液体推入瓶中 | 气球1继续微微鼓起, … | |
| ③打开K,将气球2中的固体氢氧化钠倒入瓶中后,关闭K | 气球1继续变大, … |
(2)补全步骤②中的现象:紫色石蕊溶液变红.
(3)补全步骤③中的现象:溶液由红色变为蓝色,其中“气球1继续变大”的原因是二氧化碳与氢氧化钠反应使容器内气体减少,压强减小.
(4)通过本实验能验证的二氧化碳的化学性质是二氧化碳分别能与水、氢氧化钙、氢氧化钠反应.
10.下列除去杂质的方法中,正确的是( )
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | NaCl | Na2CO3 | 适量H2SO4 |
| B | Na2NO3溶液 | Na2SO4 | 适量BaCl2、过滤 |
| C | FeCl2溶液 | CuCl2 | 过量铁粉、过滤 |
| D | 二氧化碳 | 一氧化碳 | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
17.滴有酚酞的氢氧化钡溶液与下列各物质恰好完全反应后,溶液仍显红色的是( )
| A. | CO2 | B. | Na2CO3 | C. | H2SO4 | D. | MgSO4 |
14.铁暴露在空气中会生锈.不知你注意了没有,将苹果切开不久,果肉上就会产生一层咖啡色的物质,好像是生了“锈”一样.某化学活动小组对此进行了探究.
【提出问题】切开的苹果“生锈”与什么因素有关?
【猜想与假设
猜想①:可能与空气没有关系,只是果肉内的物质自身相互反应而“生锈”.
猜想②:可能是果肉中的物质与空气中的氧气作用而“生锈”;
猜想③:可能是果肉中的物质与空气中的氮气作用而“生锈”;
猜想④:可能是果肉中的物质与空气中的二氧化碳作用而“生锈”;
猜想⑤:可能是果肉中的物质与空气中的氧气作用而“生锈”,并且苹果“生锈”的速度还可能与温度有关.
【收集证据】
(一)查阅有关资料:已知苹果“生锈”是果肉里的物质(酚和酶)与空气中的一种物质发生反应,生成咖啡色的物质.
(二)实验探究:针对上面的猜想①至猜想⑤,化学活动小组依次设计了实验方案,进行了实验验证,并依次观察到下列实验现象.请你将他们设计的可行的实验探究方案,填写在下表中.
【得出结论】切开的苹果“生锈”是果肉中的成分与氧气作用的结果;“生锈”的速度与温度有关,温度越高,果肉变色速度越快.
【反思与评价 (1)在②-⑤四种猜想中,你认为猜想2 (填代号)最不合理,理由是氮气的化学性质不活泼.
(2)在验证猜想①时,同学们发现,如果水不与空气隔绝,果肉放在水中时间长了也会变色,其可能的原因是水中能够溶解少量的氧气.
【应用】根据上述结论,要防止果汁变质,果品加工厂加工和保存果汁时可采取的措施是将水果在隔绝空气的条件下加工,采用真空包装并低温保存.
【提出问题】切开的苹果“生锈”与什么因素有关?
【猜想与假设
猜想①:可能与空气没有关系,只是果肉内的物质自身相互反应而“生锈”.
猜想②:可能是果肉中的物质与空气中的氧气作用而“生锈”;
猜想③:可能是果肉中的物质与空气中的氮气作用而“生锈”;
猜想④:可能是果肉中的物质与空气中的二氧化碳作用而“生锈”;
猜想⑤:可能是果肉中的物质与空气中的氧气作用而“生锈”,并且苹果“生锈”的速度还可能与温度有关.
【收集证据】
(一)查阅有关资料:已知苹果“生锈”是果肉里的物质(酚和酶)与空气中的一种物质发生反应,生成咖啡色的物质.
(二)实验探究:针对上面的猜想①至猜想⑤,化学活动小组依次设计了实验方案,进行了实验验证,并依次观察到下列实验现象.请你将他们设计的可行的实验探究方案,填写在下表中.
| 猜想 | 可行的实验方案 | 观察到的实验现象 |
| 猜想① | 将一小块果肉浸入盛有蒸馏水的烧杯中,观察现象. | 果肉表面不变色. |
| 猜想② | 将一小块切开的苹果放入盛有氧气的集气瓶中,观察现象. | 果肉表面变色. |
| 猜想③ | 将切开的苹果放入盛有氮气的集气瓶中,观察现象. | 果肉表面不变色. |
| 猜想④ | 果肉表面不变色. | |
| 猜想⑤ | 温度高的先变色. |
【反思与评价 (1)在②-⑤四种猜想中,你认为猜想2 (填代号)最不合理,理由是氮气的化学性质不活泼.
(2)在验证猜想①时,同学们发现,如果水不与空气隔绝,果肉放在水中时间长了也会变色,其可能的原因是水中能够溶解少量的氧气.
【应用】根据上述结论,要防止果汁变质,果品加工厂加工和保存果汁时可采取的措施是将水果在隔绝空气的条件下加工,采用真空包装并低温保存.
