题目内容
饲养观赏鱼,可以陶冶人的情操,增进人们对生活的热爱.空运观赏鱼,必须密封.为了解决鱼的吸氧问题,可在水中加入过氧化钙(化学式:CaO2),过氧化钙与水反应,生成氢氧化钙[化学式:Ca(OH)2]和氧气.
(1)已知过氧化钙,钙的化合价为+2,则氧元素的化合价为
(2)写出过氧化钙与水反应的化学方程式:
(3)一养鱼爱好者欲测定所用的过氧化钙样品中过氧化钙的质量分数(即过氧化钙质量占样品的质量的百分含量),做如下实验:称取样品2.0g,加入到足量的水中,把生成氧气全部收集起来,共有224mL.试计算所用样品中过氧化钙的质量分数.(氧气的密度为ρ=1.43g/L)
(1)已知过氧化钙,钙的化合价为+2,则氧元素的化合价为
(2)写出过氧化钙与水反应的化学方程式:
(3)一养鱼爱好者欲测定所用的过氧化钙样品中过氧化钙的质量分数(即过氧化钙质量占样品的质量的百分含量),做如下实验:称取样品2.0g,加入到足量的水中,把生成氧气全部收集起来,共有224mL.试计算所用样品中过氧化钙的质量分数.(氧气的密度为ρ=1.43g/L)
考点:有关元素化合价的计算,书写化学方程式、文字表达式、电离方程式,根据化学反应方程式的计算
专题:化学式的计算,有关化学方程式的计算,化学用语和质量守恒定律
分析:(1)根据在化合物中正负化合价代数和为零,进行解答本题.
(2)过氧化钙与水反应生成氢氧化钙和氧气,写出反应的化学方程式即可.
(3)计算样品中过氧化钙的质量分数时,根据化学方程式求出过氧化钙的质量,再除以样品的质量即可求得.
(2)过氧化钙与水反应生成氢氧化钙和氧气,写出反应的化学方程式即可.
(3)计算样品中过氧化钙的质量分数时,根据化学方程式求出过氧化钙的质量,再除以样品的质量即可求得.
解答:解:(1)钙元素显+2价,设氧元素的化合价是x,根据在化合物中正负化合价代数和为零可知CaO2中氧元素的化合价:(+2)+2x=0,则x=-1;
(2)过氧化钙与水反应生成氢氧化钙和氧气,反应的化学方程式为:2CaO2+2H2O═2Ca(OH)2+O2↑.
(3)224mL氧气质量为:1.43g/l×0.224≈0.32g,
设2.0g样品中含CaO2质量为a,则有
2CaO2+2H2O═2Ca(OH)2+O2↑
144 32
a 0.32g
=
,解得a=1.44g
样品中过氧化钙的质量分数为:
×100%=72%
答:所用样品中过氧化钙的质量分数为72%.
故填:(1)-1;(2)2CaO2+2H2O=2Ca(OH)2+O2↑;(3)72%.
(2)过氧化钙与水反应生成氢氧化钙和氧气,反应的化学方程式为:2CaO2+2H2O═2Ca(OH)2+O2↑.
(3)224mL氧气质量为:1.43g/l×0.224≈0.32g,
设2.0g样品中含CaO2质量为a,则有
2CaO2+2H2O═2Ca(OH)2+O2↑
144 32
a 0.32g
| 144 |
| a |
| 32 |
| 0.32g |
样品中过氧化钙的质量分数为:
| 1.44g |
| 2.0g |
答:所用样品中过氧化钙的质量分数为72%.
故填:(1)-1;(2)2CaO2+2H2O=2Ca(OH)2+O2↑;(3)72%.
点评:本题注意考查化学方程式的书写、样品纯度的求算,完成此题,可以依据题干提供的信息进行,书写方程式要注意配平.

练习册系列答案
相关题目
下列物质的用途,既利用了碳的物理性质,又利用了其化学性质的是( )
| A、用焦碳炼铁 |
| B、用墨写字 |
| C、用活性炭脱色 |
| D、用木炭作燃料 |
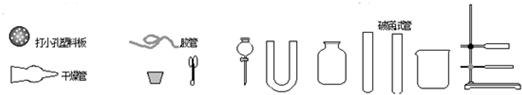


 如图所示:
如图所示: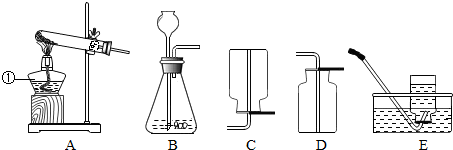
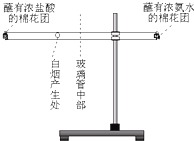 取一根长玻璃导管(两端均不封闭),固定在铁架台上,再取两团棉花,一团蘸浓氨水,另一团蘸浓盐酸,然后同时把这两团棉花分别塞在玻璃导管的两端(如图所示).一段时间后,可观察到在玻璃导管中部偏浓盐酸的位置,开始产生白烟.该实验重复几次,均观察到相似的现象.
取一根长玻璃导管(两端均不封闭),固定在铁架台上,再取两团棉花,一团蘸浓氨水,另一团蘸浓盐酸,然后同时把这两团棉花分别塞在玻璃导管的两端(如图所示).一段时间后,可观察到在玻璃导管中部偏浓盐酸的位置,开始产生白烟.该实验重复几次,均观察到相似的现象.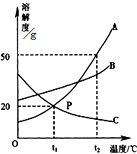 如图是A、B、C三种物质的溶解度曲线,A与C溶解度曲线相交于P点.据图回答:
如图是A、B、C三种物质的溶解度曲线,A与C溶解度曲线相交于P点.据图回答: