题目内容
铁是生活中应用最广的金属.

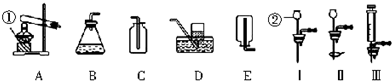
(1)如图1是探究铁制品锈蚀的条件时做的五个实验(铁钉在不同环境中),一段时间.
①甲、乙、戊中铁钉生锈快慢的顺序为: ;
②铁生锈的主要条件是:铁与 共同作用.
(2)某化学兴趣小组用一氧化碳与氧化铁的反应来探究炼铁的原理,装置如图2所示.请回答有关问题:
①为避免一氧化碳污染空气,并收集一氧化碳,方框中连接的是C和D,导管接口的连接顺序为a→ .
②C装置中NaOH的作用是 .
(3)工业上用含氧化铁64%的赤铁矿3200t,理论上可炼得含铁95%的生铁多少吨?(保留整数)

(1)如图1是探究铁制品锈蚀的条件时做的五个实验(铁钉在不同环境中),一段时间.
①甲、乙、戊中铁钉生锈快慢的顺序为:
②铁生锈的主要条件是:铁与
(2)某化学兴趣小组用一氧化碳与氧化铁的反应来探究炼铁的原理,装置如图2所示.请回答有关问题:
①为避免一氧化碳污染空气,并收集一氧化碳,方框中连接的是C和D,导管接口的连接顺序为a→
②C装置中NaOH的作用是
(3)工业上用含氧化铁64%的赤铁矿3200t,理论上可炼得含铁95%的生铁多少吨?(保留整数)
考点:金属锈蚀的条件及其防护,一氧化碳还原氧化铁,含杂质物质的化学反应的有关计算
专题:金属与金属材料
分析:根据已有的知识进行分析,铁在与水和氧气并存易生锈,酸、盐能促进铁的锈蚀;根据一氧化碳还原氧化铁的实验进行分析解答即可.
解答:解:(1)①戊是铁在干燥的空气中,不易生锈,乙是向水中通入氧气,铁与水和氧气接触的最为充分,最易生锈,故甲、乙、戊中铁钉生锈快慢的顺序为:乙>甲>戊,故填:乙>甲>戊;
②铁在与水和氧气并存易生锈,故填:氧气、水
(2)①为避免一氧化碳污染空气,并收集一氧化碳,需要将a与d相连,然后将C中的氢氧化钠溶液排出,用D承接,故填:dbe;
②氢氧化钠溶液能吸收产生的二氧化碳,故填:吸收二氧化碳;
(3)设生成生铁的质量为x
Fe2O3+3CO
2Fe+3CO2
160 112
3200t×64% 95%x
=
x=1509t
答:理论上可炼得含铁95%的生铁1509t.
②铁在与水和氧气并存易生锈,故填:氧气、水
(2)①为避免一氧化碳污染空气,并收集一氧化碳,需要将a与d相连,然后将C中的氢氧化钠溶液排出,用D承接,故填:dbe;
②氢氧化钠溶液能吸收产生的二氧化碳,故填:吸收二氧化碳;
(3)设生成生铁的质量为x
Fe2O3+3CO
| ||
160 112
3200t×64% 95%x
| 160 |
| 3200t×64% |
| 112 |
| 95%x |
x=1509t
答:理论上可炼得含铁95%的生铁1509t.
点评:本题考查了金属的锈蚀以及根据化学方程式的计算,完成此题,可以依据已有的知识进行.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案
相关题目
下列药品取用不正确的是( )
| A、取用粉末状固体药品,应该用药匙或纸槽 |
| B、为了节约药品,将用剩的药品回收,并放入原试剂瓶中 |
| C、块状固体,应该用镊子 |
| D、不要尝任何药品的味道 |
N2表示氮气,还可以表示:①氮元素,②一个氮分子,③两个氮元素,④氮气是由氮元素组成,⑤每个氮分子⑥两个氮分子,正确的是( )
| A、②④⑤ | B、①③⑤ |
| C、①②③ | D、②④⑥ |
某人将少量硝酸铜固体放入试管中加热,使之按下式反应:硝酸铜
氧化铜+二氧化氮+氧气.完全反应后立即将带火星的木条插入试管中(生成的气体中氧气的体积约占
),木条复燃.下列说法中正确的是( )
| 加热 |
| 1 |
| 5 |
| A、木条复燃只是由于反应生成了氧气 |
| B、二氧化氮不能支持燃烧 |
| C、木条复燃是反应中生成的二氧化氮和氧气与木条共同作用的结果 |
| D、木条复燃只是由于反应生成了二氧化氮 |