题目内容
4.向CuCl2、HCl组成的混合溶液中,加入一定量的铁粉,充分反应后过滤,所得滤液中只有一种溶质,下列有关该实验的叙述中,不正确的是( )| A. | 滤液一定为浅绿色溶液 | B. | 反应中一定有气体产生 | ||
| C. | 加入铁粉质量可能等于滤渣质量 | D. | 滤出的固体一定是纯净物 |
分析 铁能够和氯化铜及盐酸反应,向CuCl2、HCl组成的混合溶液中,加入一定量的铁粉,充分反应后过滤,所得滤液中只有一种溶质,说明氯化铜和盐酸都反应完了,溶质只有氯化亚铁,滤渣一定含有铜,可能含有铁,据此分析.
解答 解:铁能够和氯化铜及盐酸反应,向CuCl2、HCl组成的混合溶液中,加入一定量的铁粉,充分反应后过滤,所得滤液中只有一种溶质,说明氯化铜和盐酸都反应了,溶质只有氯化亚铁,滤渣一定含有铜,可能含有铁,因此:
A、滤液的溶质只有氯化亚铁,为浅绿色,故说法正确;
B、铁和盐酸反应产生氢气,故说法正确;
C、铁与氯化铜反应,Fe+CuCl2═FeCl2+Cu,56份的铁置换出64份质量的铜,滤渣质量会增加;铁和盐酸反应会使固体质量减少,因此滤渣质量可能等于铁粉质量,故说法正确;
D、滤渣一定含有铜,可能含有铁,可能是混合物,故说法错误;
故选项为:D.
点评 利用金属活动性顺序,可知金属的活动性;了解金属活动性顺序表的应用,并学会利用它们处理和解决问题.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
14.如图能量的转化过程中,由化学能转化为电能的是( )
| A. |  蓄电池放电 | B. |  风力发电 | C. |  水力发电 | D. |  太阳能发电 |

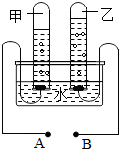 如图为电解水的实验装置图,请根据你所了解的知识填空
如图为电解水的实验装置图,请根据你所了解的知识填空 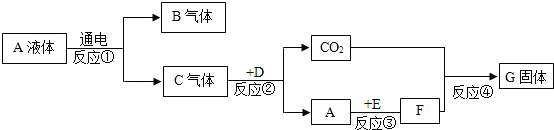
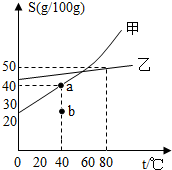 根据甲乙物质的溶解度曲线回答下列问题:
根据甲乙物质的溶解度曲线回答下列问题: