题目内容
10.美国阿拉莫斯国家实验室5月13日宣布,首次从辐照后低浓铀溶液中生产出钼-99.其中Na2MoO4是Mo元素的重要化合物,其中Mo元素的化合价是( )| A. | +7价 | B. | +6价 | C. | +5价 | D. | +4价 |
分析 根据在化合物中正负化合价代数和为零,结合物质的化学式进行解答本题.
解答 解:钠元素显+1,氧元素显-2,设钼元素的化合价是x,根据在化合物中正负化合价代数和为零,则可知Na2MoO4中Mo元素的化合价是:(+1)×2+x+(-2)×4=0,则x=+6.
故选B.
点评 本题难度不大,考查利用化合价的原则计算指定元素的化合价的能力,根据在化合物中正负化合价代数和为零计算即可.

练习册系列答案
相关题目
20.下列事实与对应的解释相符合的是( )
| A. | 空气能被压缩--分子体积可以变小 | |
| B. | 铵盐都能与氢氧化钠反应立生氨气--铵盐中含有NH4+ | |
| C. | 结冰的水不能流动--0℃以下,水分子不再运动 | |
| D. | 20mL水和20L酒精混合后的总体积小于40mL--分子的质量和体积都很小 |
18.下列物质的名称、俗称、化学式表示的是同一种物质的是( )
| A. | 氢氧化钠、纯碱、NaOH | B. | 氯化钠、食盐、NaCl | ||
| C. | 氧化钙、熟石灰、CaO | D. | 氯化氢、盐酸、HCl |
5.废物利用不仅可以保护环境,还可以节约资源,下面是某化学兴趣小组对废旧电池的回收利用,请回答下列问题.
【实验1】回收填料中的二氧化锰和氯化铵
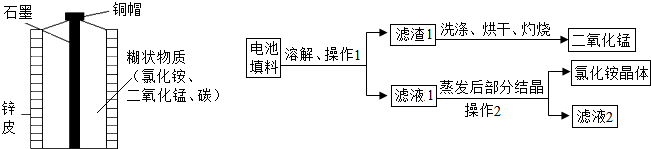
(1)操作2中玻璃棒的作用是搅拌、使液体均匀受热;
(2)灼烧滤渣1的目的是除去炭粉;
(3)在上述物质中,在实验室制取氧气的反应中可用作催化剂的是二氧化锰,含氮元素且可作氮肥的是氯化铵;
(4)在某温度下蒸发滤液 1 时,大量的氯化铵晶体析出的原因是形成了氯化铵的饱和溶液.
实验2 利用外壳回收物锌制取氢气及相关探究
(5)用锌和稀硫酸制取氢气.己知氢气密度比空气小且难溶于水.
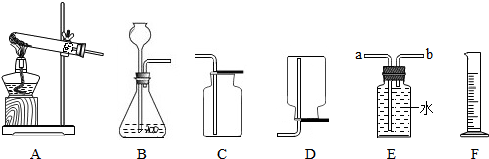
①装置选择:选择的发生装置为B(填编号),要收集比较干燥的气体,应选用的收集装置为D(填编号).
②若用排水法收集并测定气体的体积,气体从装置 E导管口b(填“a”或“b”) 进;选用仪器 F 测量排出水的体积,仪器 F 名称是量筒,若选用50ml的量筒,收集完毕量筒中剩余4ml,则收集的气体为46mL.
(6)探究影响锌与稀硫酸反应快慢的因素.如表是小明分别用相同质量的锌和足量的稀硫酸反应的四组实验数据:
①比较实验Ⅰ和实验Ⅱ,可以得到的结论是含杂质的锌与稀硫酸反应的快.
②为了研究硫酸浓度对反应快慢的影响,需比较实验Ⅱ和实验Ⅲ(填编号).
③实验Ⅲ和Ⅳ标明该反应快慢与温度有关;
④如果把实验Ⅱ中硫酸的质量分数改为4%,请你推测锌消失的时间(用t表示)的取值范围200~300
⑤该实验除了用锌消失的时间来衡量反应的快慢外,你还能提出新的方法来衡量该反应的快慢吗?相同的时间内产生的氢气的体积来衡量该反应的快慢.
【实验1】回收填料中的二氧化锰和氯化铵

(1)操作2中玻璃棒的作用是搅拌、使液体均匀受热;
(2)灼烧滤渣1的目的是除去炭粉;
(3)在上述物质中,在实验室制取氧气的反应中可用作催化剂的是二氧化锰,含氮元素且可作氮肥的是氯化铵;
(4)在某温度下蒸发滤液 1 时,大量的氯化铵晶体析出的原因是形成了氯化铵的饱和溶液.
实验2 利用外壳回收物锌制取氢气及相关探究
(5)用锌和稀硫酸制取氢气.己知氢气密度比空气小且难溶于水.
①装置选择:选择的发生装置为B(填编号),要收集比较干燥的气体,应选用的收集装置为D(填编号).
②若用排水法收集并测定气体的体积,气体从装置 E导管口b(填“a”或“b”) 进;选用仪器 F 测量排出水的体积,仪器 F 名称是量筒,若选用50ml的量筒,收集完毕量筒中剩余4ml,则收集的气体为46mL.

(6)探究影响锌与稀硫酸反应快慢的因素.如表是小明分别用相同质量的锌和足量的稀硫酸反应的四组实验数据:
| 实验序号 | 不同纯度的锌 | 硫酸的质量分数/% | 反应温度/℃ | 锌消失的时间/s |
| Ⅰ | 含杂质锌 | 3 | 20 | 200 |
| Ⅱ | 纯锌 | 3 | 20 | 500 |
| Ⅲ | 纯锌 | 6 | 20 | 300 |
| Ⅳ | 纯锌 | 6 | 30 | 80 |
②为了研究硫酸浓度对反应快慢的影响,需比较实验Ⅱ和实验Ⅲ(填编号).
③实验Ⅲ和Ⅳ标明该反应快慢与温度有关;
④如果把实验Ⅱ中硫酸的质量分数改为4%,请你推测锌消失的时间(用t表示)的取值范围200~300
⑤该实验除了用锌消失的时间来衡量反应的快慢外,你还能提出新的方法来衡量该反应的快慢吗?相同的时间内产生的氢气的体积来衡量该反应的快慢.
15.为防止实验室意外事故的发生,下列处理方法正确的是( )
| A. | 浓硫酸溅到皮肤上,立即用氢氧化钠浓溶液清洗 | |
| B. | 用高锰酸钾制氧气,当收集完氧气后,先熄灭酒精灯,再把导管从水槽中拿出 | |
| C. | 打翻燃着的酒精灯,用湿抹布盖灭 | |
| D. | 在加热试管中的液体时,为了方便观察,试管口对着自己 |
19.2014年12月7日,哥本哈根气候变化峰会试图建立一个温室气体排放的全球框架.为了不再让地球发烧,我们要倡导低碳生活的理念.下列说法不正确的是( )
| A. | 我们要养成随手关灯、拔插头的习惯 | |
| B. | 某些新建小区强制要求10层以上楼房使用太阳能热水器 | |
| C. | 将煤加工成气体和液体,以提高煤的燃烧效率 | |
| D. | 为了充分利用洗衣机的烘干功能,洗完衣服后直接烘干,无需晾晒 |
14.从化学的视角认识下列食物,其中富含蛋白质的是( )
| A. | 凉拌黄瓜 | B. | 红烧肥肉 | C. | 玉米窝头 | D. | 清蒸鱼 |