题目内容
12.硫在氧气中燃烧产生明亮的蓝紫色的火焰,硫在空气中燃烧产生微弱的淡蓝色 的火焰.反应的化学方程式为S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.生成的气体与三氧化硫具有相同的组成元素,它们具有相同的分子数时氧原子的个数比2:3; 具有相同的质量时氧元素质量比5:6.分析 根据物质的燃烧情况描述实验现象,根据质量守恒定律可以正确书写化学方程式.根据化合物中某元素的质量=该化合物的质量×该化合物中该元素的质量分数,进行解答.
解答 解:硫在氧气中燃烧的实验现象为:硫在氧气中剧烈的燃烧,发出明亮的蓝紫色火焰,放出大量的热.
硫在空气中燃烧的实验现象为:硫在空气中安静的燃烧,发出微弱的淡蓝色的火焰,放出热量.硫燃烧生成二氧化硫,反应的化学方程式为:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2
生成的气体与三氧化硫具有相同的组成元素;假设二氧化硫与三氧化硫的分子个数均为1,则二氧化硫与三氧化硫分子中氧原子的个数比2:3,
设两种物质的质量都为m,
则二氧化硫中氧元素的质量为m×$\frac{16×2}{32+16×2}×$100%=$\frac{m}{2}$
则三氧化硫中氧元素的质量为m×$\frac{16×3}{32+16×3}×$100%=$\frac{3m}{5}$
则等质量的二氧化硫和三氧化硫中氧元素的质量比为:$\frac{\frac{m}{2}}{\frac{3m}{5}}$=5:6;
答案:明亮的蓝紫色 淡蓝色 S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 组成 2:3 5:6
点评 本题考查学生对化合物中某元素的质量分数及元素质量比计算方法的掌握与在解题中灵活应用的能力.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
2.核电荷数为114的原子,其相对原子质量为289,则中子数与电子数之差为( )
| A. | 175 | B. | 114 | C. | 61 | D. | 289 |
3.下列实验现象的描述正确的是( )
| A. | 氢气在氧气中燃烧生成水 | B. | 白磷在空气中燃烧生成白色气体 | ||
| C. | 碳在氧气中燃烧生成黑色固体 | D. | 硫在空气中燃烧发出淡蓝色火焰 |
20.实验室常用的蒸馏水不是( )
| A. | 化合物 | B. | 纯净物 | C. | 混合物 | D. | 氧化物 |
7.Na+、O2-、Mg2+三种微粒的结构中不同的是( )
| A. | 核外电子数 | B. | 电子层数 | C. | 核电荷数 | D. | 最外层电子数 |
17.中考复习阶段,小荷同学梳理了以下知识:
①煮沸可以降低井水的硬度;
②某粒子的结构示意图为,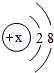 该粒子一定是氖原子;
该粒子一定是氖原子;
③二氧化碳气体可直接用作制冷剂;
④自制简易净水器中的活性炭能吸附、过滤水中的杂质;
⑤经过沉淀、过滤并加活性炭吸附后得到的水,可以直接饮用;
⑥淡化海水可解决淡水紧缺问题.其中正确的是( )
①煮沸可以降低井水的硬度;
②某粒子的结构示意图为,
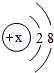 该粒子一定是氖原子;
该粒子一定是氖原子;③二氧化碳气体可直接用作制冷剂;
④自制简易净水器中的活性炭能吸附、过滤水中的杂质;
⑤经过沉淀、过滤并加活性炭吸附后得到的水,可以直接饮用;
⑥淡化海水可解决淡水紧缺问题.其中正确的是( )
| A. | ①②④⑤⑥ | B. | ②③④⑤ | C. | ①④⑤ | D. | ①④⑥ |
4.现有水(H2O)、双氧水(H2O2)、重水(D2O,“D”表示原子核中有一个质子和一个中子的氢原子)有关这三种物质的说法正确的是( )
| A. | 从化学性质上看,与水的化学性质有较大差异的是D2O | |
| B. | 从元素组成上看,这三种物质共含有3种元素 | |
| C. | 双氧水(H2O2)中氧元素化合价为-2价 | |
| D. | 从单个分子的质量上看,重水分子比水分子质量大 |
1.下列各组物质按酸、碱、单质、氧化物顺序排列的是( )
| A. | H2SO4 Na2O C CO | B. | Mg(OH)2 CuSO4 C CO2 | ||
| C. | KOH HNO3 O2 SO3 | D. | HCl NaOH O2 P2O5 |
2.如图所示的四个图象,能正确反映对应变化关系的是( )
| A. | 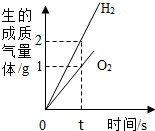 水的电解 | |
| B. | 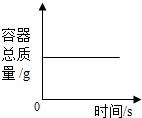 木炭在密闭的容器内燃烧 | |
| C. | 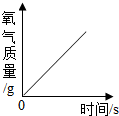 加热一定量的高锰酸钾制氧气 | |
| D. | 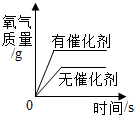 等质量的氯酸钾在有无二氧化锰条件下加热 |