题目内容
养成“规范操作、周密观察”的良好习惯,是完成化学实验的关键.
(1)如图是实验室配制50g 10%的氯化钠溶液的操作示意图,正确操作顺序为 (填字母序号);取9g上述溶液配制溶质质量分数为0.9%的生理盐水,需加水 g.
(2)为证明酸与碱能发生反应,某同学进行了以下实验,请看图回答:

①图甲:滴入酚酞试液后,观察到的现象为 ;
②图乙:用滴管慢慢滴入稀硫酸,并不断搅拌至溶液颜色恰好变成 为止;
③图丙:丙中操作存在的问题是 ;若用正确操作测得丙中溶液的pH=5,溶液中溶质的化学式为 .
| 一定溶质质量分数的溶液的配制;溶液的酸碱度测定;用水稀释改变浓度的方法;中和反应及其应用;溶液的酸碱性与pH值的关系. | |
| 专题: | 溶液、浊液与溶解度;常见的酸 酸的通性. |
| 分析: | (1) (2)①根据酚酞遇氢氧化钠变红色解答; ②酸碱中和反应的实质解答; ③根据溶液的酸碱性确定溶质的成分,和PH试纸的使用注意事项解答. |
| 解答: | 解:(1)图A则是搅拌溶解;图B为称取氯化钠的操作;图C为用药匙取出固体氯化钠准备进行称量;图D为把 取9g上述溶液配制溶质质量分数为0.9%的生理盐水,需加水: (2)①氢氧化钠溶液中滴入酚酞试液后变红色; ②稀硫酸与氢氧化钠发生酸碱中和反应,会使溶液碱性消失,溶液会有红色变为无色; ③用PH试纸测定溶液的PH时,试纸不能浸入了溶液中,会把溶液污染;测得丙中溶液的pH=5,说明溶液显酸性,及硫酸有剩余,故溶液中溶质有过剩的硫酸,以及生成的硫酸钠两种物质. 答案:(1)CBDEA,91; (2)①溶液变红色; ②无色; ③PH试纸浸入了溶液中,H2SO4,Na2SO4. |
| 点评: | 配制溶液时,先称取固体药品倒入烧杯,然后再量取水倒入烧杯,最后进行搅拌溶解. |

清华大学的同学们成功修改了“PX”的网络词条,其关键词如下:“PX”是对二甲苯的缩写,化学式为C10H8,无色液体,不溶于水,低毒性化合物.下列说法正确的是( )
|
| A. | “PX”属于碳氢化合物,能完全燃烧生成二氧化碳和水 |
|
| B. | “PX”中氢元素的质量分数大于甲烷中氢元素的质量分数 |
|
| C. | “PX”由10个碳原子和8个氢原子组成 |
|
| D. | “无色液体,不溶于水,低毒性”均属于“PX”的物理性质 |
取10g碳酸钙与溶质质量分数为10%的稀盐酸反应,恰好完全反应时间得到溶液的质量为a g;另取10g碳酸钙高温完全分解后,取生成的CaO与上述同浓度的稀盐酸反应,恰好完全反应时得到溶液的质量为b g,则a与b的大小关系为( )
|
| A. | a=b | B. | a>b | C. | a<b | D. | 不能确定 |
 观察操作图,分析每个操作的作用,根据配制溶液的步骤对操作进行排序.根据稀释溶液时溶质不变解答;
观察操作图,分析每个操作的作用,根据配制溶液的步骤对操作进行排序.根据稀释溶液时溶质不变解答; 称量的氯化钠倒入烧杯;图E为量取一定量的水倒入烧杯;则正确的操作顺序为:CBDEA;
称量的氯化钠倒入烧杯;图E为量取一定量的水倒入烧杯;则正确的操作顺序为:CBDEA;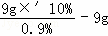 =91g
=91g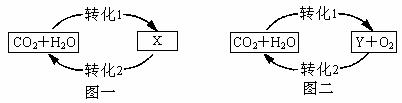

 方法制备并收集干燥的氧气.
方法制备并收集干燥的氧气.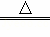 2Fe+3H2O;其中D1、D2、D3为三个浓硫酸洗气瓶)
2Fe+3H2O;其中D1、D2、D3为三个浓硫酸洗气瓶)