题目内容
6. 在测定硫酸铜晶体中结晶水的含量实验中,某同学用如图所示装置完成了实验.根据实验过程回答下列问题:
在测定硫酸铜晶体中结晶水的含量实验中,某同学用如图所示装置完成了实验.根据实验过程回答下列问题:①写出图中标有字母仪器的名称:
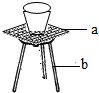
a石棉网,b铁三角架.
②实验中取用坩埚时要用坩埚钳,仪器a在实验中的作用是使仪器受热均匀.
③实验过程中观察到的现象是有白雾产生,蓝色晶体变成白色粉末.
分析 ①根据实验室常用仪器解答;
②根据实验中取用坩埚时要用坩埚钳解答;
③硫酸铜晶体失去结晶水变为白色粉末解答.
解答 解:①根据实验室常用仪器可知:a石棉网,b铁三角架;
②实验中取用坩埚时要用坩埚钳;石棉网在实验中的作用是使仪器受热均匀;
③硫酸铜晶体在加热过程中,现象是有白雾产生,蓝色晶体变成白色粉末.
答案:
①石棉网,铁三角架;
②坩埚钳;使仪器受热均匀;
③有白雾产生,蓝色晶体变成白色粉末.
点评 本题难度不大,主要考查实验室常用仪器的识别和用途,熟练掌握有关知识是正确解答的依据.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
20.判断下列说法中正确的是( )
| A. | 20℃时,100g水里最多能溶解36g氯化钠,所以20℃时氯化钠的溶解度为36g | |
| B. | 20℃时,硝酸钾的溶解度为31.6 | |
| C. | 20℃时,在100g水中加入35g氯化钠完全溶解,则20℃时,氯化钠的溶解度为35g | |
| D. | 20℃时,100g氯化钠的饱和溶液中有27g氯化钠,则20℃时,氯化钠的溶解度为27g |
14.“黄金有价玉无价”,某种玉石的主要成分是NaAlSi2O6,下列说法正确的是( )
| A. | 这种玉石含有4种元素 | |
| B. | 这种玉石的主要成分含有10个原子 | |
| C. | 这种玉石主要成分中硅元素化合价为+3 | |
| D. | 这种玉石主要成分中硅元素化合价为+6 |
1.下列关于溶解度的说法正确的是( )
| A. | 100克水溶解20克某物质刚好饱和,则该物质的溶解度为20克 | |
| B. | 20℃时,100克水中溶解了10克某物质,则20℃时该物质的溶解度为10克 | |
| C. | 20℃时,50克水最多可以溶解18克食盐,则20℃时食盐的溶解度为18克 | |
| D. | 20℃时,100克水溶解32克硝酸钾恰好达到饱和,则20℃时该物质的溶解度为32克 |
11.下列属于化学变化的是( )
| A. | 海水晒盐 | B. | 酚酞遇碱变红 | C. | 盐酸挥发 | D. | 干冰升华 |
 人类的生活和生产都离不开金属材料.
人类的生活和生产都离不开金属材料.