题目内容
正确的实验操作是进行科学实验的重要保障.下列操作中,合理的是( )
|
| A. | 少量酒精在实验台上燃烧时,立即用湿抹布盖灭 |
|
| B. | 稀释浓硫酸时,将水注入盛有浓硫酸的烧杯中 |
|
| C. | 测定某溶液的pH时,先用水将pH试纸润湿 |
|
| D. | 向试管中滴加液体时,将胶头滴管伸入试管内 |
| 加热器皿-酒精灯;液体药品的取用;浓硫酸的性质及浓硫酸的稀释;溶液的酸碱度测定. | |
| 专题: | 常见仪器及化学实验基本操作. |
| 分析: | A、从少量酒精在实验台上燃烧时,可能会引起失火,应立即用湿抹布盖灭去分析解答; B、从稀如果将水注入浓硫酸里,由于水的密度较小,水会浮在浓硫酸的上面,溶解时放出的热量能使水立刻沸腾,使硫酸液滴向四周飞溅,这是非常危险的去分析解答. C、从先用水将pH试纸润湿,相当于把待测液加水稀释,可能改变了溶液的酸碱度去分析解答; D、从向试管中滴加液体时,胶头滴管要竖直、悬空、不能伸入试管内去分析解答; |
| 解答: | 解:A、少量酒精在实验台上燃烧时,可能会引起失火,应立即用湿抹布盖灭;故A正确; B、稀释浓硫酸时,应把浓硫酸沿器壁慢慢注入水中,同时用玻璃棒不断搅拌,切不可把水倒进浓硫酸里;如果将水注入浓硫酸里,由于水的密度较小,水会浮在浓硫酸的上面,溶解时放出的热量能使水立刻沸腾,使硫酸液滴向四周飞溅,这是非常危险的.故B错误; C、先用水将pH试纸润湿,相当于把待测液加水稀释,可能改变了溶液的酸碱度,故C错误; D、向试管中滴加液体时,胶头滴管要竖直、悬空、不能伸入试管内;故D错误; 故答案为:A. |
| 点评: | 化学是一门以实验为基础的科学,学好实验基本操作是做好化学实验的基础. |

 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案某同学设计了以下三个实验,要证明Cu、Zn、Ag的活动性顺序,必须要做的实验是( )
|
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
某同学为研究相同条件下一氧化碳和氢气哪个还原氧化铁的量更多,将一氧化碳和氢气等体积混合后先通过图甲装置,再通过图乙中的仪器组合。为达到实验目的,图乙中仪器选择和连接最好的是
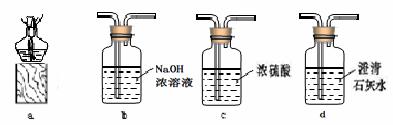
|
|
A.cba B.cda C.cbd D.bca
小明把过量锌粒加入有盐酸的试管中,发现随着反应的进行,产生气体的速度逐渐加快,一段时间后逐渐减慢,最后停止产生气体。在反应 过程中,溶液的温度也先随之升高,最后下降到室温。于是,小明设计实验来探究“一定质量的某种金属和同体积盐酸反应快慢的影响因素”。测得实验数据如下:
过程中,溶液的温度也先随之升高,最后下降到室温。于是,小明设计实验来探究“一定质量的某种金属和同体积盐酸反应快慢的影响因素”。测得实验数据如下:
某金属与同体积盐酸溶液反应实验数据表
| 盐酸溶液浓度 | 反应开始时酸 溶液的温度 | 反应开始到2分钟产生的气体体积 | 反应结束共产生气体体积 |
| 5% | 20℃ | 10 mL | 60 mL |
| 10% | 20℃ | 19 mL | 118 mL |
| 15% | 20℃ | 28 mL | 175 mL |
| 5% | 35℃ | 28 mL | 60 mL |
| 10% | 35℃ | 72 mL | 118 mL |
| 15% | 35℃ | 103 mL | 175 mL |
(1)分析实验数据得出:一定质量的某种金属和同体积盐酸反应,影响金属和酸反应快慢的主要因素有 、 。
(2)可以通过比较 实验数据来确定金属和酸反应的快慢。
(3)过量锌粒加入盐酸中,反应开始的一段时间,反应速率逐渐加快,而不是逐渐减慢。请分析原因。 。
除去下列各物质中混有的少量杂质(括号内为杂质),下列方法中,不正确的是( )
|
| A. | 铜粉(CuO)﹣﹣加入过量的稀硫酸,过滤 |
|
| B. | H2(HCl)﹣﹣通过足量的氢氧化钠溶液,干燥 |
|
| C. | NaCl溶液(Na2SO4)﹣﹣加入适量的Ba(NO3)2溶液,过滤 |
|
| D. | CaCl2溶液(HCl)﹣﹣加入过量的碳酸钙粉末,过滤 |

