题目内容
下列对相应微粒的描述中,不正确的是( )
|
| A. | 易失电子 | B. | 易形成阴离子 | C. | 带正电荷 | D. | 化学性质稳定 |
| 原子结构示意图与离子结构示意图.. | |
| 专题: | 化学用语和质量守恒定律. |
| 分析: | 根据已有的知识进行分析,核内质子数=核外电子数是原子,核内质子数>核外电子数是阳离子,核内质子数<核外电子数是阴离子,最外层电子数小于4个易是电子,大于4个易得电子,等于8个是稳定结构,据此解答. |
| 解答: | 解:A、该原子的最外层电子数是1,易失去电子,故A正确; B、该原子最外层电子数是6,易得电子,形成阴离子,故B正确; C、该微粒核内质子数<核外电子数是阴离子,带负电荷,故C错误; D、该原子最外层电子数是8,是稳定结构,化学性质稳定,故D正确; 故选C. |
| 点评: | 本题考查了微粒结构示意图的知识,完成此题,可以依据已有的原子结构示意图的有关知识进行. |

丽丽的爸爸旅游归来,带回一些钟乳硒石块送给了她.丽丽和同学们想验证钟 乳石的主要成分是碳酸盐,于是她们将其中一块钟乳石带进实验室进行探究.(1)请你帮助丽丽完成以下探究方案.
乳石的主要成分是碳酸盐,于是她们将其中一块钟乳石带进实验室进行探究.(1)请你帮助丽丽完成以下探究方案.
| 实验操作 | 预期的实验现象 | 实验结论 |
| ①取一小块钟乳石于试管中,向试管中 加入 ,观察现象. ② ,观察现象. | 有气泡生成
| 钟乳石的主要 成分是碳酸盐 |
(2)查阅资料得知钟乳石的主要成分是碳酸钙(假设杂质不溶于水且不与酸发生反应).上述预期的实验现象中有气泡生成的反应的化学方程式为
(3)实验后,为了防止废液腐蚀下水管道或对水质产生不良影响,丽丽将所有的废液倒入了一个洁净的烧杯中.她取样测定了废液的酸碱性,你认为她选择的试剂可以是 .测试后得知该废液显酸性,则烧杯中废液的溶质是 
(4)丽丽向烧杯中的废液里加入过量的 (填序号)能使废液呈中性,过滤后才可安全排放. ①碳酸钙 ②熟石灰 ③生石灰 ④氢氧化钠.
生活中处处离不开化学知识,下列说法中,错误的是( )
|
| A. | 春天,花儿朵朵,由于分子在不停运动我们能闻到花香 |
|
| B. | 夏天,烈日炎炎,用可乐等碳酸饮料替代饮水有利于身体健康 |
|
| C. | 秋天,果实累累,多吃水果可以补充人体所需的多种维生素 |
|
| D. | 冬天,寒风冽冽,室内用煤炉取暖应保证烟囱通畅,防止“煤气”中毒 |
配制50g溶质的质量分数为6%的氯化钠溶液,不需要的仪器是( )
|
| A. | 蒸发皿 | B. | 玻璃棒 | C. | 烧杯 | D. | 量筒 |
化学反应前后,下列各项中,肯定没有变化的是( )
①原子数目 ②原子的种类 ③分子数目 ④分子的种类 ⑤元素的种类 ⑥物质的总质量 ⑦物质的种类.
|
| A. | ①②⑤⑥ | B. | ①②③⑤ | C. | ①②⑤⑦ | D. | ③④⑥⑦ |
以下物质不作为空气污染物计入《环境空气质量标准》基本检测的是( )
|
| A. | 二氧化碳 | B. | 二氧化氮 | C. | 一氧化碳 | D. | PM2.5 |
小亮同学阅读课外资料得知:氧化铜和氧化铁等金属氧化物也可以作为过氧化氢溶液分解制取氧气的催化剂,于是他选择氧化铜进行了探究实验.
【提出问题】氧化铜是否可以做过氧化氢溶液分解制取氧气的催化剂呢?它是否比二氧化锰催化剂效果更好呢?
【设计实验】小亮以生成40mL的氧气为标准,设计了如下实验:
| 实验序号 | 5%过氧化氢溶液体积/mL | 其他物质 | 产生40mL氧气所用的时间 |
| ① | 10 | / | |
| ② | 10 | 氧化铜1.2g | |
| ③ | 10 | 二氧化锰1.2 |
(1)该实验中,测量氧气的体积应选择的装置是 (填序号).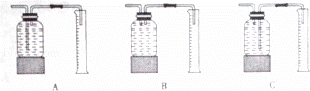
(2)若实验②产生40mL氧气比实验①的时间更 (填“多”或“少”),说明氧化铜能加快氧化氢分解速率.
(3)若要证明氧化铜是过氧化氢分解制取氧气的催化剂,还需要验证氧化铜在实验②中反应前后的 未发生改变,小亮同学将实验②反应后的固体进行过滤、洗涤,再称量得到1.2g黑色粉末,再将黑色粉末加入试管中, .(简述操作和现象).
(4)若产生40mL,氧气实验②的时间大于实验③,则可以得出 .
【预期结论】 .
