题目内容
15. 回答下列有关Zn、Fe、Cu、Ag的相关问题:
回答下列有关Zn、Fe、Cu、Ag的相关问题:(1)实验一的实验现象是A、B两支试管中均有气体产生,且B比A反应快,此实验不可以(“可以”或“不可以”)证明铁和锌的活动性强弱.
(2)实验二的结论是三种金属活动性由强到弱的顺序是铁、铜、银.
分析 (1)根据金属活动性顺序进行分析;
(2)根据铁会与硫酸铜反应,铜会与硝酸银反应进行分析.
解答 解:(1)铁、锌都会与酸反应,但是锌比铁活泼,反应速率快,所以实验一的实验现象是A、B两支试管中均有气体产生,且B比A反应快,两种金属反应的酸不相同,所以该实验不可以证明铁和锌的活动性强弱;
(2)铁会与硫酸铜反应,铁比铜活泼,铜会与硝酸银反应,铜比银活泼,所以实验二的结论是:三种金属活动性由强到弱的顺序是铁、铜、银.
故答案为:(1)A、B两支试管中均有气体产生,且B比A反应快,不可以;
(2)三种金属活动性由强到弱的顺序是铁、铜、银.
点评 要会利用金属活动顺序表设计实验,去验证金属的活动性强弱.氢前边的金属会与酸反应,但氢后边的金属不会与酸反应,验证三种金属活动性顺序类问题时,一般采取“三取中”的方法进行设计实验,即选取活动性位于中间的那种金属的单质与另两种金属的盐溶液反应;或取中间金属的盐溶液与另两种金属的单质进行反应.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.下列不符合“低碳生活”这一主题的做法是( )
| A. | 用布袋代替一次性塑料袋购物 | B. | 使用节能灯泡,提倡节约用电 | ||
| C. | 增加私家车用量,提高生活质量 | D. | 大力发展风能,减少火力发电 |
7.把6.2g红磷放在给定的氧气中充分燃烧,实验数据如表:
(1)这三次实验数据,哪一次符合质量守恒定律?为什么?
(2)第一次实验为什么不生成10.2g的P2O5?
(3)第二次实验为什么不生成24.2g的P2O5?
| 实验 | 第一次 | 第二次 | 第二次 |
| 给定O2的质量(g) | 4 | 18 | 8 |
| 生成P2O5的质量(g) | 7.1 | 14.2 | 14.2 |
(2)第一次实验为什么不生成10.2g的P2O5?
(3)第二次实验为什么不生成24.2g的P2O5?
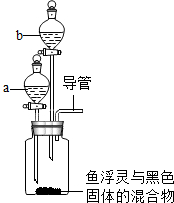 据调查,目前市场有一种产品叫“鱼浮灵”,放在鱼缸中可使水中的含氧量增加,某校科学小组的成员对“鱼浮灵”成分进行探究.
据调查,目前市场有一种产品叫“鱼浮灵”,放在鱼缸中可使水中的含氧量增加,某校科学小组的成员对“鱼浮灵”成分进行探究.