题目内容
【题目】某同学使用如图所示装置试验一氧化碳与氧化铜的反应.回答下列有关问题.
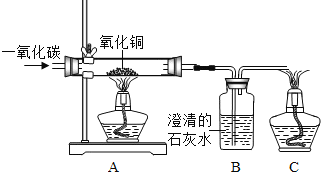
(1)实验开始时,应先_____,然后_____.
(2)实验进行一段时间后,![]() 装置中出现的现象为_____,说明有_____生成;
装置中出现的现象为_____,说明有_____生成;![]() 装置中出现的现象为_____,(用方程式表示):_____.右边酒精灯的作用为_____
装置中出现的现象为_____,(用方程式表示):_____.右边酒精灯的作用为_____
(3)由上述实验可知,一氧化碳具有____性.在我们已经学习过的物质中,具有这种性质的还有___和____.
【答案】通入一氧化碳排净玻璃管中的空气 再加热 黑色粉末变红 铜 澄清的石灰水变浑浊 ![]() 点燃尾气中的一氧化碳防止污染空气 还原 木炭 氢气
点燃尾气中的一氧化碳防止污染空气 还原 木炭 氢气
【解析】
(1)一氧化碳具有可燃性,点燃一氧化碳和空气或氧气的混合气体可能会发生爆炸,因此实验开始要先通入一氧化碳,排净玻璃管内的空气,防止加热时发生爆炸.然后再点燃酒精灯加热;
(2)一氧化碳与氧化铜反应生成铜和二氧化碳,生成的二氧化碳与氢氧化钙反应生成了碳酸钙沉淀和水.所以,![]() 装置中可看到黑色粉末变红红,说明有铜生成;
装置中可看到黑色粉末变红红,说明有铜生成;![]() 装置中出现的现象为:澄清的石灰水变浑浊,氢氧化钙与二氧化碳反应产生碳酸钙沉淀和水的方程式是:
装置中出现的现象为:澄清的石灰水变浑浊,氢氧化钙与二氧化碳反应产生碳酸钙沉淀和水的方程式是:![]() ;由于一氧化碳有毒能污染空气.所以,右边酒精灯的作用为点燃尾气中的一氧化碳,防止污染空气;
;由于一氧化碳有毒能污染空气.所以,右边酒精灯的作用为点燃尾气中的一氧化碳,防止污染空气;
(3)在上述反应中,一氧化碳能夺取氧化铜中的氧,具有还原性.在我们已经学习过的物质中,具有这种性质的还有木炭和氢气.

 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
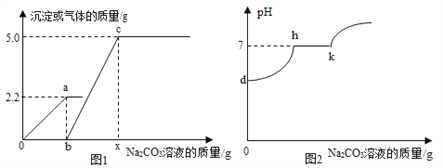
百强名校期末冲刺100分系列答案【题目】等差量的铁粉与过量的盐酸在不同的实验条件下进行反应,测定在相同时间t产生气体体积V的数据,根据数据绘制得到图1。
组别 | 盐酸的溶质质量分数 | 温度(℃) |
1 | 7 | 30 |
2 | 10 | 50 |
3 | 7 | 20 |
4 | 10 | 30 |

(1)请写出铁粉稀盐酸反应的化学方程式__________________________。
(2)由实验_________(填组别)可知,温度对于金属与酸反应速率的影响是_____。
(3)图1中表示第3组实验的曲线是____________。
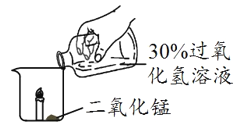
[进一步探究]图甲、图乙为利用数字化仪器测得的室温下足量的三种金属片分别与200ml100℅的稀盐酸反应产生氢气的量。(产生氢气的量由气体压强表示,在等温条件下,产生氢气体积与装置内压强成正比)。

①实验中你认为,还要控制的变量是_________________________。
②由图乙,你得出的反应物的量与生成的气体体积的关系是____________。
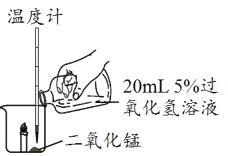
[拓展提高]下图为测得的室温下足量的镁片与20ml110℅的稀盐酸反应产生氢气的量与时间关系曲线,发现实验测得的实际值比通过计算得到的理论值偏大,请分析可能的原因(至少答两点)。

①_______________________________。
②________________________________________。
【题目】某化学实验小组利用蜡烛进行了下列实验。
实验1:
序号 | 1-1 | 1-2 | 1-3 |
操作 |
|
|
|
现象 | 燃烧的蜡烛保持原状 | 燃烧的蜡烛熄灭 | 剧烈反应,有大量气泡和水雾生成,燃烧的蜡烛熄灭了 |
(1)实验1-2中,燃烧的蜡烛熄灭的原因是____。
(2)实验1-3中,反应生成氧气的化学方程式为___。
实验2:
(提出问题)实验1-3中燃烧的蜡烛为什么会熄灭?
(猜想与假设)
I.蜡烛燃烧生成的二氧化碳导致其熄灭。
II.过氧化氢分解时吸收热量,蜡烛周围的温度降低到着火点以下,导致其熄灭。
III.过氧化氢分解产生的水雾导致蜡烛熄灭。
(进行试验)
序号 | 2-1 | 2-2 | 2-3 |
操作 |
|
|
|
现象 | 有气泡产生,蜡烛火焰无明显变化,温度升高不明显 | 有较多气泡和少量水雾产生,蜡烛燃烧更旺。火焰明亮,温度升高较明显 | 剧烈反应,有大量气泡和水雾产生,燃烧的蜡烛熄灭,温度升高明显 |
(解释与结论)
(3)甲同学认为猜想I不成立,他的依据是____。
(4)通过实验验证,可以得出猜想____(填序号)成立。
(5)上述实验中,能证明氧气有助燃性的实验及现象是____。
(反思与评价)
(6)依据上述实验,若保持实验1-3中蜡烛不熄灭,可采用的方法有___。