题目内容
1.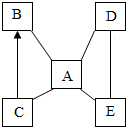 A、B、C、D、E为初中化学常见的五种不同类别的物质,其中C为红棕色固体,D可用于改良酸性土壤,它们之间的转化关系如图所示,请回答问题:(“-”表示能相互反应,“→”表示能够转化,其中部分反应物、生成物和反应条件已略去)
A、B、C、D、E为初中化学常见的五种不同类别的物质,其中C为红棕色固体,D可用于改良酸性土壤,它们之间的转化关系如图所示,请回答问题:(“-”表示能相互反应,“→”表示能够转化,其中部分反应物、生成物和反应条件已略去)(1)D的化学式是HCl,A与D反应的基本类型是复分解反应.
(2)A与B反应的现象是有气泡产生,溶液由无色变为浅绿色.
(3)C→B的化学方程式是Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(4)A与E反应的化学方程式是Na2CO3+2HCl=2NaCl+H2O+CO2↑.
分析 根据A、B、C、D、E为初中化学常见的五种不同类别的物质,D可用于改良酸性土壤,所以D是氢氧化钙,属于碱,C是红棕色固体,则C是氧化铁,属于氧化物,氧化铁、氢氧化钙会与A反应,所以A可以是盐酸,属于酸,氧化铁转化成的B会与盐酸,所以B是铁,属于单质,盐酸、氢氧化钙会与E反应,所以E是盐,可以是碳酸钠,然后将推出的物质进行验证即可.
解答 解:(1)A、B、C、D、E为初中化学常见的五种不同类别的物质,D可用于改良酸性土壤,所以D是氢氧化钙,属于碱,C是红棕色固体,则C是氧化铁,属于氧化物,氧化铁、氢氧化钙会与A反应,所以A可以是盐酸,属于酸,氧化铁转化成的B会与盐酸,所以B是铁,属于单质,盐酸、氢氧化钙会与E反应,所以E是盐,可以是碳酸钠,经过验证,推导正确,所以D是HCl,A与D的反应是氢氧化钠和盐酸反应生成氯化钠和水,所以基本反应类型是复分解反应;
(2)A与B的反应是铁和盐酸反应生成氯化亚铁和氢气,实验现象是:有气泡产生,溶液由无色变为浅绿色;
(3)C→B的反应是氧化铁和一氧化碳在高温的条件下生成铁和二氧化碳,化学方程式是:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(4)A与E的反应是碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,化学方程式是:Na2CO3+2HCl=2NaCl+H2O+CO2↑.
故答案为:(1)HCl,复分解反应;
(2)有气泡产生,溶液由无色变为浅绿色;
(3)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(4)Na2CO3+2HCl=2NaCl+H2O+CO2↑.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

| A. | H2--2个氢元素 | B. | O2--2个氧原子 | ||
| C. | $\stackrel{+2}{Mg}$--1个镁离子 | D. | CO2--1个二氧化碳分子 |
 液化石油气是经加压后压缩袋钢瓶中的,瓶内压强是大气压强的7-8倍.液化石油气的主要成分是丙烷、丁烷、丙烯和丁烯等.下列有关丁烷的叙述正确的是( )
液化石油气是经加压后压缩袋钢瓶中的,瓶内压强是大气压强的7-8倍.液化石油气的主要成分是丙烷、丁烷、丙烯和丁烯等.下列有关丁烷的叙述正确的是( )| A. | 丁烷中碳、氢元素的个数比为2:5 | B. | 丁烷分子中氢元素的质量分数最大 | ||
| C. | 丁烷是由碳、氢原子构成的有机物 | D. | 在通常状况下,丁烷是气体 |
| A. | 滤渣是Ag、Cu、Zn | B. | 滤液中含有Zn2+、Mg2+、NO3- | ||
| C. | 滤渣是Ag、Cu、Mg | D. | 金属活动性顺序是Ag<Cu<Zn<Mg |
| A. | 由14个原子构成 | |
| B. | 其中碳元素的质量分数为41.4% | |
| C. | 其中碳、氢、氧元素的质量比为12:1:16 | |
| D. | 一个乙酸乙酯分子中,碳、氢、氧原子的个数比为2:4:1 |
| A. | 工业中为节约生产成本,多用化石燃料 | |
| B. | 学生实验后将污水倒入下水道 | |
| C. | 化工厂未经处理排放废水 | |
| D. | 提倡植树造林,禁止乱砍滥伐 |
| A. | 石蕊试液 | B. | Na2CO3溶液 | C. | Fe2(SO4)3溶液 | D. | Cu(NO3)2溶液 |
 汽车方便了人们的出行.氢能源汽车备受人们关注
汽车方便了人们的出行.氢能源汽车备受人们关注