题目内容
18.请写出实现下列转化的四个反应的化学方程式: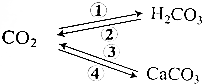
①CO2+H2O═H2CO3②H2CO3═H2O+CO2↑③CaCO3+2HCl=CaCl2+H2O+CO2↑④CO2+Ca(OH)2═CaCO3↓+H2O.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:①二氧化碳与水反应生成碳酸,反应的化学方程式为:CO2+H2O═H2CO3.
②碳酸分解生成水和二氧化碳,反应的化学方程式为:H2CO3═H2O+CO2↑.
③碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑.
④二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O.
故答案为:①CO2+H2O═H2CO3;②H2CO3═H2O+CO2↑;③CaCO3+2HCl=CaCl2+H2O+CO2↑;④CO2+Ca(OH)2═CaCO3↓+H2O.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
8.在M+2O2═CO2+2H2O中,依质量守恒定律,可判断M为( )
| A. | CH3OH | B. | C2H5OH | C. | CH3COOH | D. | CH4 |
9.某省盛产石灰石,其中含有杂质为二氧化硅(不溶水).某中学初三研究小组的同学为了测定某矿山石灰石的纯度(碳酸钙的质量分数),取4.0g该矿山石灰石样品,将50g盐酸平均分成5份,分5次加入到样品中,数据见下表:
(1)五次实验中,盐酸完全反应的有第1、2、3 次(填写实验的次数).
(2)石灰石样品中碳酸钙的质量分数.
(3)此种盐酸里的氯化氢气体的质量分数.
| 实验次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 加入盐酸质量/g | 10 | 10 | 10 | 10 | 10 |
| 每次产生气体质量/g | 0.44 | 0.44 | 0.44 | 0.22 | 0 |
(2)石灰石样品中碳酸钙的质量分数.
(3)此种盐酸里的氯化氢气体的质量分数.
4.要除去二氧化碳中的少量的一氧化碳,可以把混合气体( )
| A. | 通过澄清的石灰水 | B. | 通过灼热的氧化铜 | ||
| C. | 点燃 | D. | 从一个容器倒入另一个容器 |
9.某化学兴趣小组的同学对碳酸钙高温加热一段时间剩余固体的成分进行探究.
提出问题:剩余固体成分是什么?
猜想与假设:剩余固体成分为:A.全部是碳酸钙 B.既有碳酸钙,也有氧化钙 C.氧化钙
设计并完成实验
实验结论:该化学兴趣小组同学得出的结论:剩余固体成分与“猜想与假设”中的B(填“A”或“B”或“C”)吻合.
交流与反思:剩余固体的成分若与C相符,则两步操作的实验现象(2)(填“(1)”或“(2)”或“(1)(2)”)不同.
提出问题:剩余固体成分是什么?
猜想与假设:剩余固体成分为:A.全部是碳酸钙 B.既有碳酸钙,也有氧化钙 C.氧化钙
设计并完成实验
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体于试管中,加适量水振荡后静置,再滴几滴无色酚酞试液 | 溶液变红 | 说明固体成分中一定含有 氧化钙 |
| (2)再取少量固体于另一试管中滴加过量稀盐酸 | 有气泡生成 | 说明固体成分中一定含有 碳酸钙 |
交流与反思:剩余固体的成分若与C相符,则两步操作的实验现象(2)(填“(1)”或“(2)”或“(1)(2)”)不同.
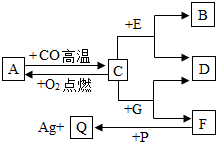 现有A、B、C、D、E、F、G、P、Q九种物质,其中A为磁铁矿的主要成分,C、F是常见金属,B是相对分子质量最小的气体单质,D为浅绿色溶液,G为蓝色溶液.它们之间关系如图所示,试推测:
现有A、B、C、D、E、F、G、P、Q九种物质,其中A为磁铁矿的主要成分,C、F是常见金属,B是相对分子质量最小的气体单质,D为浅绿色溶液,G为蓝色溶液.它们之间关系如图所示,试推测: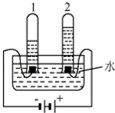 水是一种重要的资源.
水是一种重要的资源.