题目内容
2014年“六•五”世界环境日中国的主题为“向污染宣战”。下列做法符合这一主题的是
A.通过焚烧秸杆为农作物提供养分 B.通过加高烟囱排放工业废气
C.提倡步行、骑自行车等“低碳”出行方式 D.施用大量的化肥和农药以提高农作物产量
C

 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案| 分子、原子、离子、元素与物质之间的关系;原子的定义与构成;原子和离子的相互转化.. | |
| 专题: | 物质的微观构成与物质的宏观组成. |
| 分析: | A、根据原子的定义来解答该题; B、根据离子的形成分析回答; C、分子之间有间隔,这是分子普遍具有的性质; D、构成物质的基本微粒有分子、原子和离子.可以根据微观粒子的性质和构成方面进行分析、判断,从而得出正确的结论;原子由核外电子和原子核构成,构成物质的微粒有分子、原子和离子,原子得失电子变成离子,微粒之间有间隔. |
| 解答: | 解:A、原子是化学变化中的最小粒子,但并不意味着原子就是最小的粒子,原子还可以继续被分成更微小的粒子,如质子、中子、电子;故A错误; B、钠原子失去一个电子变为钠离子,其质子数不变,所以钠原子的质子数等于钠离子的质子数;故B错误; C、任何物质的分子之间都有间隔,本题中氧气变成液氧只是分子间的间隔变小,但是间隔依然存在,故C错误; D、分子、原子和离子都可以直接构成物质,它们是构成物质的三种基本微粒,故D正确; 故选D. |
| 点评: | 本题主要考查了微观粒子的特征、性质和构成等方面的内容,可以依据已有知识进行分析解答. |
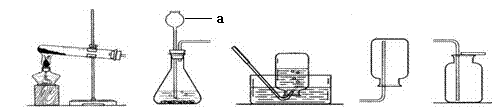 工业上常用分离液态空气法制取氧气,实验室常用物质分解的方法制氧气。某校化学兴趣小组的同学根据实验室提供的仪器和药品,在老师的指导下从下图中选择装置进行了氧气的制备实验。
工业上常用分离液态空气法制取氧气,实验室常用物质分解的方法制氧气。某校化学兴趣小组的同学根据实验室提供的仪器和药品,在老师的指导下从下图中选择装置进行了氧气的制备实验。
B C D
A B C D E
(1)(2分)工业制氧气是 (填“物理”或“化学”)变化,仪器a的名称是: 。
(2)(4分)甲同学从上图中选择B、E装置的组合制取氧气,反应的符号表达为: 。反应类型为( )收集氧气还可选用的装置是 。
(3)(3分)若用装置B制氧气,反应通常很剧烈,据此提出实验安全注意事项是( )
A.更换部分仪器,控制液体的加入速度 B.用体积小的广口瓶
C.加热反应物 D.减小过氧化氢浓度
(4)(2分)氨气极易溶于水,且密度比空气小,实验室常用加热固体硫酸铵和固体熟石灰的混合物来制取氨气,应选用上图 作发生装置,收集氨气最好用上图 装置。
(5)(4分)乙同学称取一定质量的KMnO4固体放入大试管中,将温度控制在250℃加热制取O2.实验结束时,乙同学发现收集到的O2大于理论产量.针对这一现象,同学们进行了如下探究:
【提出猜想】猜想Ⅰ:反应生成的MnO2分解放出O2;
猜想Ⅱ:反应生成的K2MnO4分解放出O2;
猜想Ⅲ:反应生成的K2MnO4和MnO2分解放出O2.
【实验验证】同学们分成两组,分别进行下列实验:第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变,则猜测 错误;第二组同学取K2MnO4在250℃条件下加热,没有用测定质量的方法得出了猜想Ⅱ正确的结论.该组同学选择的实验方法是 。
(6)(5分)丙同学阅读课外资料得知:双氧水分解除了用二氧化锰还可用氧化铜等物质作催化剂,于是他对氧化铜产生了探究兴趣,请你一起参与实验探究,并填写下列空白:。
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】丙同学以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略)。
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| ① | 1.2g | ////////////// | |
| ② | 1.2g | CuO 0.5g | |
| ③ | 1.2g | MnO2 0.5g |
(Ⅰ)上述实验应测量的“待测数据”是 。
(Ⅱ)若实验②比实验①的“待测数据”更 (填“大”或“小”),说明氧化铜能加快氯酸钾的分解速率。
(Ⅲ)将实验②反应后的固体加水溶解、过滤、洗涤、干燥,若测量得到0.5g氧化铜( CuO )粉末,再将黑色粉末放入试管中, 。(简述操作和现象)
【预期结论】氧化铜还能作氯酸钾分解的催化剂。
【评价设计】你认为丙同学设计实验③和实验②对比的目的是 。
漂白粉在生活生产中有重要的应用.氯气与石灰乳反应制得漂白粉的化学方程式为2Cl2+2Ca(OH)2═Ca(ClO)2+X+2H2O,其中X的化学式是( )
|
| A. | CaO | B. | CaH2 | C. | Ca(ClO3)2 | D. | CaCl2 |