题目内容
10.请回答下列有关的问题.(1 )在水的净化过程中,常利用活性炭的吸附性除去异味和有色物质;
(2)日常生活中,用肥皂水来区分硬水和软水;
(3 )天然存在的硬度最大的物质的名称是金刚石.
(4)CO和C02都是碳的氧化物,但由于它们的分子构成不同.导致化学性质不同,用点燃的方法鉴别它们时,有关反应的化学方程式为2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.
分析 (1)根据活性炭的吸附性除去异味解答;
(2)根据肥皂水可区分软水和硬水解答;
(3)根据天然存在的硬度最大的物质的名称是金刚石解答;
(4)根据一氧化碳和二氧化碳的分子构成不同,一氧化碳具有可燃性,二氧化碳不具有可燃性,据此解答.
解答 解:
(1)活性炭具有吸附性,在水的净化过程中,常利用活性炭的吸附性除去异味和有色物质;
(2)软水加入肥皂水后,产生的泡沫较多;硬水加入肥皂水后,产生的泡沫少,所以用肥皂水可以区分软水和硬水,故填:肥皂水;
(3)天然存在的硬度最大的物质的名称是金刚石;
(4)一氧化碳和二氧化碳的分子构成不同,因而化学性质不同,一氧化碳能与氧气点燃生成二氧化碳,故填:分子构成,2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.
答案:
(1)活性炭;
(2)肥皂水;
(3)金刚石;
(4)分子构成;2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.
点评 软水、硬水的区分,活性炭的吸附性,水的组成都是基础知识,所以同学们都应掌握好基础知识,以不变应万变.

练习册系列答案
相关题目
1.小明在实验室发现一瓶氢氧化钠固体没有塞上瓶塞,于是他和他的同学一起对这瓶氢氧化钠固体展开探究,请你与他们一起进行探究.
【提出问题】这瓶氢氧化钠固体是否变质?
【猜想与假设】
①氢氧化钠没有变质;②该氢氧化钠部分变质;③该氢氧化钠全部变质.
【设计实验】取氢氧化钠固体样品溶于水配成溶液A,进行如下实验:
【反思与交流】
(4)久置的氢氧化钠变质的原因是(用化学方程式表示)CO2+2NaOH=Na2CO3+H2O.
【探索与拓展】为进一步探究氢氧化钠的变质程度,小明称取18.6g氢氧化钠固体样品放入烧杯中,向其中逐滴加入稀盐酸,到不再产生气泡为止,共消耗稀盐酸100g,反应后称得烧杯中溶液的质量为114.2g.
(5)求该样品中碳酸钠的质量(要写出计算过程);
(6)该氢氧化钠的变质程度(即变质的氢氧化钠占变质前的氢氧化钠的质量分数)为50%.
【提出问题】这瓶氢氧化钠固体是否变质?
【猜想与假设】
①氢氧化钠没有变质;②该氢氧化钠部分变质;③该氢氧化钠全部变质.
【设计实验】取氢氧化钠固体样品溶于水配成溶液A,进行如下实验:
| 实验步骤 | 实验现象 | 结论及解释 |
| (1)取少量溶液A于试管中,向其中滴加足量的稀盐酸; | 有气泡产生 | 猜想①不成立 |
| (2)另取少量溶液A于试管中,向其中滴加足量的氯化钙溶液; | 产生白色沉淀 | 反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl |
| (3)将步骤(2)所得的混合液静置,向上层清液中滴加无色的酚酞溶液. | 溶液呈红色 | 猜想②成立 |
(4)久置的氢氧化钠变质的原因是(用化学方程式表示)CO2+2NaOH=Na2CO3+H2O.
【探索与拓展】为进一步探究氢氧化钠的变质程度,小明称取18.6g氢氧化钠固体样品放入烧杯中,向其中逐滴加入稀盐酸,到不再产生气泡为止,共消耗稀盐酸100g,反应后称得烧杯中溶液的质量为114.2g.
(5)求该样品中碳酸钠的质量(要写出计算过程);
(6)该氢氧化钠的变质程度(即变质的氢氧化钠占变质前的氢氧化钠的质量分数)为50%.
5.下列有关环境和能源的说法中,错误的是( )
| A. | 生活污水应集中处理达标后排放 | |
| B. | 煤、石油、天然气都属于不可再生能源,都是纯净物 | |
| C. | 使用乙醇汽油可以节省石油资源,减少汽车尾气污染环境 | |
| D. | 二氧化碳含量增大会使温室效应加剧,但是它不属于空气污染物 |
2.下列有关氧气的说法正确的是( )
| A. | 夏天食物腐烂与氧气无关 | |
| B. | 氧化反应一定是化合反应 | |
| C. | 氧气具有可燃性 | |
| D. | 增加氧气的浓度,能促进可燃物的燃烧 |
19.下列实验及操作正确的是( )
| A. |  闻气体的气味 | B. | 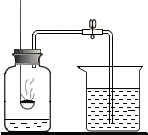 拉瓦锡验证空气组成 | ||
| C. |  用镊子取食盐 | D. | 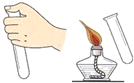 检验氢气纯度 |
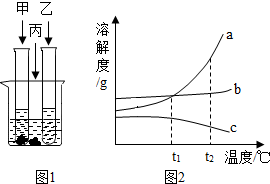 在室温下,甲、乙、丙三种固体分别溶于两支试管和一个烧杯的水中,现象如图1所示,甲、丙还有剩余固体,乙固体全部溶解.升温到80℃时,发现甲固体全部溶解,乙固体析出,丙固体没有明显变化.
在室温下,甲、乙、丙三种固体分别溶于两支试管和一个烧杯的水中,现象如图1所示,甲、丙还有剩余固体,乙固体全部溶解.升温到80℃时,发现甲固体全部溶解,乙固体析出,丙固体没有明显变化.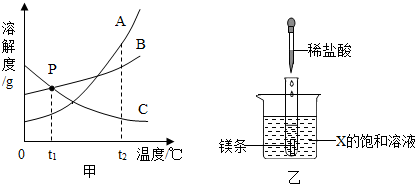
 (1)酒精灯不使用时,为什么要用灯帽将酒精灯盖灭而不能用嘴吹灭?
(1)酒精灯不使用时,为什么要用灯帽将酒精灯盖灭而不能用嘴吹灭?