题目内容
6.镁能与NH4C1溶液反应,不仅生成一种盐,还有气泡产生.为确定气体的成分,某化学兴趣小组的同学进行下列实验探究.【提出问题】镁能与NH4C1溶液反应生成何种气体?
【猜想与假设】小华说:生成气体可能是HCl、NH3、H2中的一种或几种
(1)小华作出上述猜想的理论依据是化学反应前后元素种类不变;
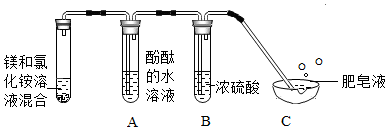
【进行实验】修正后该小组同学认为:该气体可能含有NH3和H2或NH3,他们设计如下装置进行实验:
【现象与结论】
(2)A中观察到酚酞试液变红,证明生成气体含有NH3:B装置中浓硫酸的作用:①干燥气体;②吸收NH3:C中有肥皂泡飘到空中,用燃着的木条靠近肥皂泡,有爆呜声,说明生成的气体还含有氢气.
【实验反思】(3)写出Mg与NH4C1溶液反应的化学方程式Mg+2NH4Cl=MgCl2+2NH3↑+H2↑.
(4)氨气极易溶于水,上述实验中有氨气逸出的原因可能是此反应放热,降低了氨气的溶解度.
分析 【猜想与假设】根据质量守恒定律来分析;
【现象与结论】氨水显碱性,能使酚酞试液变红色;浓硫酸具有吸水性,能和氨气反应生成硫酸铵;
氢气密度小,具有可燃性解答;
【实验反思】
(3)根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式;
(4)根据镁和氯化铵反应放热分析.
解答 解:【猜想与假设】由质量守恒定律可知,化学反应前后元素的种类不变,所以猜想可能是HCl、NH3、H2中的一种或几种,故填:化学反应前后元素种类保持不变;
【现象与结论】
B中观察到酚酞试剂变红色,证明产生的气体中有一种能与水反应生成碱性物质,则为氨气,因为氨气与水反应生成氨水,氨水是一种碱,能使无色酚酞试液变红色;浓硫酸有吸水性,同时能和氨气反应生成硫酸铵;D肥皂泡飘到空气中,用燃着的木条靠近肥皂泡,有爆鸣声,生成的气体中含有氢气;
【实验反思】
(3)Mg与NH4Cl溶液反应生成MgCl2、NH3和H2,反应的化学方程式为:Mg+2NH4Cl═MgCl2+2NH3↑+H2↑.
(4)氨气极易溶于水,上述实验中A装置有氨气逸出的原因可能是该反应放热,温度升高,使氨气在水中的溶解度减小.
答案:
(1)化学反应前后元素种类不变
(2)酚酞试液变红;吸收NH3;氢气;
(3)Mg+2NH4Cl=MgCl2+2NH3↑+H2↑;
(4)此反应放热,降低了氨气的溶解度.
点评 本题是一道实验和结论相结合的题目,可以根据所学知识来回答,难度不大.实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目
7.空气中,主要与维持自然生态平衡的“碳-氧循环”有关的气体是( )
| A. | O2和CO2 | B. | H2O和CO2 | C. | O2和N2 | D. | CO2和N2 |
8.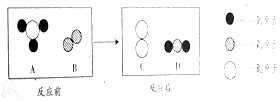 点燃条件下,物质A与B反应生成C和D,反应前后分子种类变化的微观示意图如图,下列说法不正确的是( )
点燃条件下,物质A与B反应生成C和D,反应前后分子种类变化的微观示意图如图,下列说法不正确的是( )
 点燃条件下,物质A与B反应生成C和D,反应前后分子种类变化的微观示意图如图,下列说法不正确的是( )
点燃条件下,物质A与B反应生成C和D,反应前后分子种类变化的微观示意图如图,下列说法不正确的是( )| A. | 化学反应前后原子的种类不变 | |
| B. | 该反应中,生成物C与D的质量比为2:3 | |
| C. | 反应物和生成物中共有2种单质 | |
| D. | 原子是化学变化中最小微粒 |
5.用数轴表示某些化学知识直观、简明、易记.下列数轴表示的化学知识不正确的是( )
| A. | 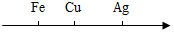 金属活动性由弱到强 | |
| B. |  液体的pH值由低到高 | |
| C. |  氯元素的化合价由低到高 | |
| D. |  常温常压下气体在水中的溶解性由弱到强 |
18.分类是学习和研究化学常用的方法.下列关于物质分类中正确的是( )
| A. | 混合物:煤、石油、冰水混合物 | B. | 有机物:甲烷、乙醇、葡萄糖 | ||
| C. | 酸:硫酸、盐酸、碳酸钠 | D. | 单质:干冰、金刚石、氧气 |
16. 如图是a,b,c三种物质的溶解度曲线,下列分析不正确的是( )
如图是a,b,c三种物质的溶解度曲线,下列分析不正确的是( )
 如图是a,b,c三种物质的溶解度曲线,下列分析不正确的是( )
如图是a,b,c三种物质的溶解度曲线,下列分析不正确的是( )| A. | t2℃时,a,b,c三种物质的溶解度由大到小的顺序是a>b>c | |
| B. | t2℃时,将50g a物质放入100g水中充分溶解得到a的饱和溶液 | |
| C. | t1℃时 a,b,c三种物质的溶液中溶质质量分数关系是b>a=c | |
| D. | 除去a中少量的c,可采用降温结晶的方法 |
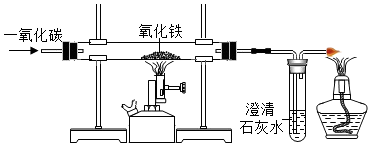 早在春秋战国时期,我国就开始生产和使用铁器.工业上炼铁的原理是利用一氧化碳和氧化铁的反应.某化学兴趣小组利用下图装置进行实验探究,请按要求填空:
早在春秋战国时期,我国就开始生产和使用铁器.工业上炼铁的原理是利用一氧化碳和氧化铁的反应.某化学兴趣小组利用下图装置进行实验探究,请按要求填空: