题目内容
12.推理是一种重要的化学思想方法,以下推理合理的是( )| A. | 分子、原子都是不带电的微粒,但不带电的微粒不一定是分子、原子 | |
| B. | 因为燃烧需要同时满足三个条件,所以灭火也需要同时控制这三个条件 | |
| C. | 氢氧化铝可以治疗胃酸过多,故氢氧化钠也可以治疗胃酸过多 | |
| D. | 化学变化都遵循质量守恒定律,所以质量不发生改变的变化就是化学变化 |
分析 A、从中子也是不带电的微粒去分析;
B、从灭火只需要控制这三个条件中的一个即可去分析;
C、从氢氧化钠具有强烈的腐蚀性去分析;
D、从质量不发生改变的变化不一定是化学变化,如糖溶于水,质量不会变,但属于物理变化去分析;
解答 解:A、分子、原子都是不带电的微粒,但不带电的微粒不一定是分子、原子.如中子也是不带电的微粒;故正确;
B、灭火只需要控制这三个条件中的一个即可;故错误;
C、氢氧化钠具有强烈的腐蚀性,不能用于治疗胃酸过多;故错误;
D、质量不发生改变的变化不一定是化学变化,如糖溶于水,质量不会变,但属于物理变化;故错误;
故答案为:A.
点评 本题综合性强,主要考查了分子、原子的构成、灭火原理、碱的性质、质量守恒定律的应用等,熟练掌握上述概念的内涵和外延是解题的关键.

练习册系列答案
相关题目
2.为研究NaOH与盐酸的反应,同学们用以下试剂设计不同方案进行探究.
实验试剂:镁条、蒸馏水、稀盐酸、NaOH溶液、NaCl溶液等
(1)小明取少量NaOH溶液于试管中,滴入酚酞,溶液变红,再滴加稀盐酸,振荡,红色褪去,可推断NaOH与盐酸发生了反应.反应的化学方程式为NaOH+HCl═NaCl+H2O.
(2)小刚取体积相同的稀盐酸分别于甲、乙两支试管中,向甲中先加1mL水,充分混合后再放入镁条,向乙中先加入1mL NaOH溶液,充分混合后再放入镁条.观察到甲中有气泡冒出.乙中无气泡(或气泡少),可推断NaOH与盐酸发生了反应.
(3)小华利用溶液导电性进行实验.分别测定几种试剂的导电性,获得相关数据:
查阅资料:
Ⅰ.溶液中若存在自由移动的离子,通电时就会发生定向移动,从而形成了电流.
Ⅱ.相同电压下,等体积溶液中,所含离子数目越多,电流就越大.
①对比实验A、C的数据,可推知NaOH溶液中除水分子外还含有自由移动的Na+和OH-(填化学符号).
②实验B、D中电流强度相等,说明等体积的稀盐酸和NaCl溶液中所含Cl-的数目相等(填写“相等”或“不相等”).
③各取10mL NaOH溶液于两个小烧杯中,分别加入10mL NaCl溶液和10mL稀盐酸(所得混合溶液体积均约为20mL),测两种混合溶液的导电性,电流示数依次为I1和I2.根据I1> I2(填“>”、“<”或“=”),也可推断氢氧化钠和盐酸发生了反应.
实验试剂:镁条、蒸馏水、稀盐酸、NaOH溶液、NaCl溶液等
(1)小明取少量NaOH溶液于试管中,滴入酚酞,溶液变红,再滴加稀盐酸,振荡,红色褪去,可推断NaOH与盐酸发生了反应.反应的化学方程式为NaOH+HCl═NaCl+H2O.
(2)小刚取体积相同的稀盐酸分别于甲、乙两支试管中,向甲中先加1mL水,充分混合后再放入镁条,向乙中先加入1mL NaOH溶液,充分混合后再放入镁条.观察到甲中有气泡冒出.乙中无气泡(或气泡少),可推断NaOH与盐酸发生了反应.
(3)小华利用溶液导电性进行实验.分别测定几种试剂的导电性,获得相关数据:
| 实验序号 | A | B | C | D |
| 试剂 | 蒸馏水 | 稀盐酸 | NaOH溶液 | NaCl溶液 |
| 电流强度/mA | 约为0 | 0.09 | 0.09 | 0.09 |
Ⅰ.溶液中若存在自由移动的离子,通电时就会发生定向移动,从而形成了电流.
Ⅱ.相同电压下,等体积溶液中,所含离子数目越多,电流就越大.
①对比实验A、C的数据,可推知NaOH溶液中除水分子外还含有自由移动的Na+和OH-(填化学符号).
②实验B、D中电流强度相等,说明等体积的稀盐酸和NaCl溶液中所含Cl-的数目相等(填写“相等”或“不相等”).
③各取10mL NaOH溶液于两个小烧杯中,分别加入10mL NaCl溶液和10mL稀盐酸(所得混合溶液体积均约为20mL),测两种混合溶液的导电性,电流示数依次为I1和I2.根据I1> I2(填“>”、“<”或“=”),也可推断氢氧化钠和盐酸发生了反应.
3.在生产水泥的过程中,要大量优质的石灰水,某学校的课外兴趣小组的同学为了测定某工厂的石灰石中碳酸钙的质量分数,取石灰石样品与足量的稀盐酸在烧杯中反应,(杂质不反应也不溶于水)有关数据如下表:
请完成下列问题:
(1)生成气体的质量为3.3g
(2)计算该石灰石样品中碳酸钙的质量分数.
| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 133.4克 | 10克 | 140.1克 | |
(1)生成气体的质量为3.3g
(2)计算该石灰石样品中碳酸钙的质量分数.
7.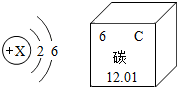 如图分别是R元素的原子结构示意图及碳元素在元素周期表中的相关信息,下列说法错误的是( )
如图分别是R元素的原子结构示意图及碳元素在元素周期表中的相关信息,下列说法错误的是( )
 如图分别是R元素的原子结构示意图及碳元素在元素周期表中的相关信息,下列说法错误的是( )
如图分别是R元素的原子结构示意图及碳元素在元素周期表中的相关信息,下列说法错误的是( )| A. | X=8 | |
| B. | 碳元素的相对原子质量为12.01 | |
| C. | 两种元素形成化合物的化学式可能是CR2 | |
| D. | R元素形成的离子符号是R4+ |
4.下列实验现象描述正确的是( )
| A. | 氢气在空气中燃烧产生淡蓝色火焰 | |
| B. | 红磷在空气中燃烧,产生白雾 | |
| C. | 铁在纯氧中剧烈燃烧、火星四射,生成四氧化三铁 | |
| D. | 木炭在氧气中完全燃烧,生成能使澄清石灰水变浑浊的二氧化碳气体 |
1.最近科学家发现,水在-157℃超低温、正常压力或真空集条件下仍呈液态,比蜂蜜还粘稠,下列关于这种“高密度液态水”的说法正确的是( )
| A. | 化学性质与普通水不同 | B. | 分子不再运动 | ||
| C. | 分子间的间隔比普通水大 | D. | 氢、氧两种原子的个数比为2:1 |