题目内容
4.0.2%~0.5%的过氧乙酸(CH3COOOH)溶液是一种杀菌能力强的高效消毒剂.(1)过氧乙酸分子中 C、H、O 原子个数比为2:4:3;
(2)过氧乙酸中元素质量分数最大为氧;
(3)欲配置 0.4%的过氧乙酸溶液 1000g,需用 20%的过氧乙酸溶液20g.
分析 (1)根据化学式的意义来分析;(2)根据化学式能计算物质中某元素的质量比,通过比较找出质量分数最大的元素;(3)根据溶液稀释过程中,溶质的质量不变来分析解答.
解答 解:(1)由过氧乙酸的化学式可知,1个过氧乙醇分子中含有2个碳原子、4个氢原子和3个氧原子,故填:2:4:3;
(2)在过氧乙酸中,碳元素、氢元素、氧元素的质量比为:(12×2):(1×4):(16×3)=24:4:48,可见过氧乙酸中氧元素的质量分数最大;
(3)设需要20%的过氧乙酸溶液的质量为x,则1000g×0.4%=20%×x,解得x=20g.
故答案为:(1)2:4:3;(2)氧;(3)20.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
19.下列实验操作正确的是( )
| A. | 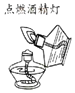 | B. |  | C. | 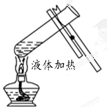 | D. |  |
20.下列物质的用途不正确的是( )
| A. | 生石灰用于食品干燥剂 | B. | 稀有气体可制成霓虹灯 | ||
| C. | 小苏打用于治疗胃酸过多 | D. | 烧碱可用于改良酸性土壤 |
12.下面是空气污染指数与空气质量级别、质量状况的关系表:
据测定,某地区的空气污染指数为68,该地区的空气质量级别和空气质量状况分别是( )
| 空气污染指数 | 0-50 | 51-100 | 101-200 | 201-300 | >300 |
| 空气质量状况 | 优 | 良 | 轻度污染 | 中度污染 | 重度污染 |
| 空气质量级别 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ |
| A. | Ⅰ级 优 | B. | Ⅱ级 良 | C. | Ⅲ级 轻度污染 | D. | Ⅴ级 重度污染 |
9.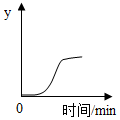 已知:CO+CuO $\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.如图表示向一定质量的CuO中通入CO后,加热的过程中,某变量y随时间的变货趋势.y表示的是( )
已知:CO+CuO $\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.如图表示向一定质量的CuO中通入CO后,加热的过程中,某变量y随时间的变货趋势.y表示的是( )
 已知:CO+CuO $\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.如图表示向一定质量的CuO中通入CO后,加热的过程中,某变量y随时间的变货趋势.y表示的是( )
已知:CO+CuO $\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.如图表示向一定质量的CuO中通入CO后,加热的过程中,某变量y随时间的变货趋势.y表示的是( )| A. | 参与反应的CO的质量 | B. | 固体中铜元素的质量分数 | ||
| C. | 固体中氧元素的质量 | D. | 气体中碳元素的质量 |
16.下列操作正确的是( )
| A. | 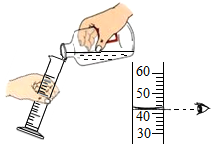 倾倒量取液体体积 | B. |  检查装置气密性 | ||
| C. | 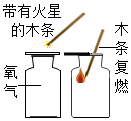 氧气的验满 | D. | 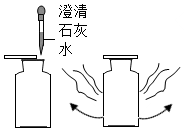 滴加澄清石灰水 |
14.下列变化中,属于化学变化的是( )
| A. | 干冰升华 | B. | 铜丝折弯 | C. | 纸张燃烧 | D. | 酒精挥发 |