题目内容
16.3.2g某有机物在足量的氧气中充分燃烧,生成了4.4gCO2和3.6g H2O,则该有机物中( )| A. | 一定含有C、H、O元素 | B. | 只含有C、H元素,不含O元素 | ||
| C. | 一定含有C、H元素,可能含O元素 | D. | 一定含有C、O元素,可能含H元素 |
分析 化学反应前后,元素的种类不变,原子的种类、总个数不变;
化学反应遵循质量守恒定律,即参加反应的物质的质量之和,等于反应后生成的物质的质量之和.
解答 解:4.4g二氧化碳中碳元素的质量为:4.4g×$\frac{12}{44}$×100%=1.2g;3.6g水中氢元素的质量为:3.6g×$\frac{2}{18}$×100%=0.4g;
二氧化碳中的碳元素和水中的氢元素来自于该有机物,该有机物中氧元素的质量为:3.2g-1.2g-0.4g=1.6g,
因此该有机物中含有碳元素、氢元素和氧元素.
故选:A.
点评 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
6.下列说法中正确的是( )
| A. | NaOH和MgO以任意质量比混合,所得混合物中氧元素的质量分数一定为40% | |
| B. | 一定量的氯化钠溶液恒温蒸发5g水,析出ag晶体;再蒸发5g水,又析出bg晶体,则a与b一定相等 | |
| C. | 用CO完全还原一定质量的CuO,参加反应的CO与所通入的CO质量一定相等 | |
| D. | 将98%的浓H2SO4用水稀释成49%的H2SO4溶液,加水的体积与浓硫酸的体积一定相等 |
6.下列说法正确的是( )
| A. | 镁条燃烧后生成的质量比镁条质量大,不符合质量守恒定律 | |
| B. | 水加热沸腾一段时间质量减少,符合质量守恒定律 | |
| C. | 4g碳和8g氧气完全反应生成12g二氧化碳 | |
| D. | 煤燃烧变成煤灰,质量变轻,符合质量守恒定律 |
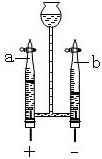 某同学制作了如图所示的简易电解水装置,进行家庭小实验(注:该装置气密性良好,且反应一段时间后停止通电)请根据要求回答问题:
某同学制作了如图所示的简易电解水装置,进行家庭小实验(注:该装置气密性良好,且反应一段时间后停止通电)请根据要求回答问题: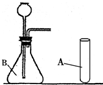 小龙同学想通过实验制取并验证二氧化碳气体.请回答下列问题:
小龙同学想通过实验制取并验证二氧化碳气体.请回答下列问题: