题目内容
17.如图是某离子的结构示意图,下列关于该离子的描述正确的是( )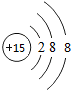
| A. | 该离子最外层电子未达到稳定结构 | B. | 属于稀有气体元素 | ||
| C. | 核电荷数为15 | D. | 最外层电子数为18 |
分析 原子结构示意图中,圆圈内数字表示核内质子数,弧线表示电子层,弧线上的数字表示该层上的电子数,离圆圈最远的弧线表示最外层.若最外层电子数≥4,在化学反应中易得电子,若最外层电子数<4,在化学反应中易失去电子.
解答 解:A、该离子的最外层电子数是8,达到稳定结构,故选项说法错误.
B、该原子的核内质子数为15,为磷元素,属于非金属元素的原子,故选项说法错误.
C、圆圈内的数字是15,表示核电荷数为15,故选项说法正确.
D、该原子的最外层电子数是8,故选项说法错误.
故选:C.
点评 本题难度不大,考查学生对原子结构示意图及其意义的理解,了解原子结构示意图的意义是正确解题的关键.

练习册系列答案
相关题目
7.利用生物发光现象可检测“超微量钙”,此处“钙”是指( )
| A. | 元素 | B. | 单质 | C. | 原子 | D. | 分子 |
8. 某品牌洁厕灵的成分是硫酸与盐酸的混合溶液.某课外活动小组想测定20g该品牌洁厕灵中H2SO4A的质量.取20g洁厕灵于烧杯中,不断滴加溶质质量分数为17.1%的氢氧化钡溶液,烧杯中产生沉淀质量和烧杯中溶液pH变红的部分数据如表所示:(已知BaCl2溶液的pH=7)
某品牌洁厕灵的成分是硫酸与盐酸的混合溶液.某课外活动小组想测定20g该品牌洁厕灵中H2SO4A的质量.取20g洁厕灵于烧杯中,不断滴加溶质质量分数为17.1%的氢氧化钡溶液,烧杯中产生沉淀质量和烧杯中溶液pH变红的部分数据如表所示:(已知BaCl2溶液的pH=7)
请结合表格和图形回答下列问题:
(1)当氢氧化钡溶液滴加到20g时,硫酸反应完全;
(2)当氢氧化钡溶液滴加到40g时溶液中存在的离子有钡离子、氢离子、氯离子;
(3)20g该品牌洁厕灵溶液中H2SO4的质量为多少克?
 某品牌洁厕灵的成分是硫酸与盐酸的混合溶液.某课外活动小组想测定20g该品牌洁厕灵中H2SO4A的质量.取20g洁厕灵于烧杯中,不断滴加溶质质量分数为17.1%的氢氧化钡溶液,烧杯中产生沉淀质量和烧杯中溶液pH变红的部分数据如表所示:(已知BaCl2溶液的pH=7)
某品牌洁厕灵的成分是硫酸与盐酸的混合溶液.某课外活动小组想测定20g该品牌洁厕灵中H2SO4A的质量.取20g洁厕灵于烧杯中,不断滴加溶质质量分数为17.1%的氢氧化钡溶液,烧杯中产生沉淀质量和烧杯中溶液pH变红的部分数据如表所示:(已知BaCl2溶液的pH=7)| 滴加氢氧化钡溶液的质量/g | 5 | 10 | 25 |
| 烧杯中产生沉淀的质量/g | 1.165 | 2.33 | 4.66 |
(1)当氢氧化钡溶液滴加到20g时,硫酸反应完全;
(2)当氢氧化钡溶液滴加到40g时溶液中存在的离子有钡离子、氢离子、氯离子;
(3)20g该品牌洁厕灵溶液中H2SO4的质量为多少克?
5.下列化学方程式书写完全正确的是( )
| A. | 2H2O═2H2↑+O2↑ | B. | Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 | ||
| C. | 3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 | D. | CO2+C$\frac{\underline{\;高温\;}}{\;}$CO |
12. 甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )
 甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )| A. | 甲的溶解度大于乙的溶解度 | |
| B. | 降低温度可使甲的不饱和溶液变为饱和溶液 | |
| C. | t1℃时,甲、乙两种溶液的溶质质量分数相等 | |
| D. | t2℃时,不可能制得相同浓度的甲和乙的溶液 |
2.Fe2+和Fe3+属于同种元素,因为它们具有相同的( )
| A. | 核电荷数 | B. | 相对原子质量 | C. | 最外层电子数 | D. | 中子数 |
9.Na2CO3是常用的化工原料,下列说法正确的是( )
| A. | Na2CO3中钠、碳、氧三种元素的质量比为2:1:3 | |
| B. | Na2CO3中C元素的质量分数为$\frac{12}{23+12+16}$×100% | |
| C. | Na2CO3溶液中含有Na+、C2-和O2- | |
| D. | Na2CO3的相对分子质量为106 |
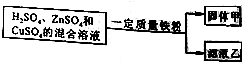 兴趣小组同学做了如图所示实验.
兴趣小组同学做了如图所示实验.