题目内容
1.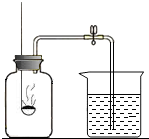 如图所示装置可用来测定空气中氧气的含量.以下实验操作与出现的实验现象和结果分析不合理的是( )
如图所示装置可用来测定空气中氧气的含量.以下实验操作与出现的实验现象和结果分析不合理的是( )| A.实验前在集气瓶内未加入少量水 | 点燃的红磷伸入集气瓶后瓶底会炸裂 |
| B.点燃红磷前未用止水夹夹紧导管 | 瓶内减少的气体体积大于五分之一 |
| C.燃烧匙插入集气瓶太慢 | 瓶内减少的气体体积大于五分之一 |
| D.红磷换用硫 | 瓶内减少的气体体积小于五分之一 |
| A. | A | B. | B | C. | C | D. | D |
分析 本题是用红磷测定空气中氧气的含量,本探究实验一般要注意以下几点:①装置的气密性好;②所用药品红磷的量,必须是足量;③读数时一定要冷却到原温度;④生成物的状态一般要求是固态等.如果控制不好条件,进入集气瓶中水体积会小于五分之一.如果装置内的部分空气逸散出来,就会导致进入集气瓶中水体积大于五分之一.
解答 解:A、红磷燃烧产生白烟,不会使集气瓶底部炸裂,故分析错误;
B、点燃红磷前未用止水夹夹紧导管,会使部分空气进入空气中,使瓶内减少的气体体积大于五分之一,故分析正确;
C、燃烧匙插入集气瓶太慢,会使集气瓶内的空气进入空气,瓶内减少的气体体积大于五分之一,故分析正确;
D、硫燃烧产生的二氧化硫是气体,因此集气瓶内的气体减少的要小于五分之一,故分析正确;
故选项为:A.
点评 本考点是测定氧气在空气中的体积分数,属于与课本知识同类信息.本探究实验在不同版本的教材中用的实验装置是不一样的,不论用哪一套装置,其原理是一致的,问题也是大同小异,就是为了证明氧气约占空气体积的五分之一的.希望同学们认真把握.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
11.请根据表中物质回答下列有关问题
(1)上表中的物质属于氧化物的是Fe2O3(用化学式表示).
(2)选用表中的物质作为反应物,写出制取氢氧化钠的化学方程式:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
| 序号 | ① | ② | ③ | ④ |
| 物质 | 醋酸 | 氧化铁 | 熟石灰 | 纯碱 |
(2)选用表中的物质作为反应物,写出制取氢氧化钠的化学方程式:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
16.简单原子的原子结构可用下图形象地表示:其中 表示质子或电子,○表示中子.则下列有关①②③的叙述中,正确的是( )
表示质子或电子,○表示中子.则下列有关①②③的叙述中,正确的是( )

 表示质子或电子,○表示中子.则下列有关①②③的叙述中,正确的是( )
表示质子或电子,○表示中子.则下列有关①②③的叙述中,正确的是( )
| A. | ①②③互为同位素 | B. | ①②③的核电荷数不同 | ||
| C. | ①②③是三种性质不同的粒子 | D. | ①②③具有相同的质量数 |
12.下列关于溶液的说法中正确的是( )
| A. | 溶液是无色的 | B. | 溶液一定是混合物 | ||
| C. | 稀溶液中含有的溶质一定少 | D. | 均一、稳定的液体一定是溶液 |
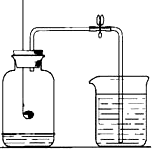 空气中氧气含量的测定实验如图:
空气中氧气含量的测定实验如图: