题目内容
某校化学实验室废液桶中收集了溶解大量FeSO4、CuSO4的废水,若直接排放到下水道不仅造成重金属污染而且造成浪费.初三(2)班的同学,准备运用刚学到的“常见金属活动性顺序表”结合其他有关化学知识对废水进行处理.
(1)复习常见金属活动顺序表,在下表空格中分别填入对应的元素符号.
K Ca Mg Al Fe Sn Pb (H) Cu Hg Pt

(2)设计除去铜离子,回收硫酸亚铁晶体和铜的实验方案,讨论有关问题:
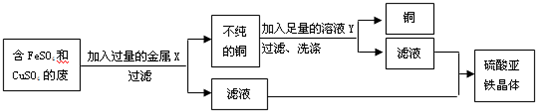
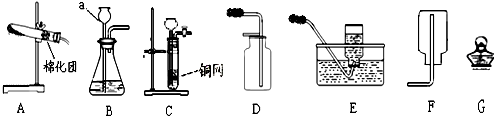
①废水在加入金属X前需进行过滤,目的是将其中 性杂质除去.进行过滤的操作所需的仪器有: 、 、 、 (请从下图中选择合适仪器,并用仪器名称填写).

②金属X是 ,其加入废水后发生反应的化学方程式为 ;溶液Y是 ,利用其除去铜中杂质,有关反应的化学方程式为 .
③从滤液中获取硫酸亚铁晶体的操作方法是 .
(1)复习常见金属活动顺序表,在下表空格中分别填入对应的元素符号.
K Ca

(2)设计除去铜离子,回收硫酸亚铁晶体和铜的实验方案,讨论有关问题:

①废水在加入金属X前需进行过滤,目的是将其中

②金属X是
③从滤液中获取硫酸亚铁晶体的操作方法是
考点:金属的化学性质,过滤的原理、方法及其应用,结晶的原理、方法及其应用,金属活动性顺序及其应用,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)根据金属活动性顺序表的内容,在空格中填入金属元素的符号.
(2)①依据混合物分离的方法分析判断操作A,根据玻璃棒的应用分析其作用;
②由于目的是获得铜单质和硫酸亚铁,所以需要将铜离子转化为铜单质,而溶液中需要的是硫酸亚铁而不能引入新的杂质,所以加入的能够将铜离子转化为铜单质的只能是单质铁;由于加入的铁是过量的,需要加入过量稀硫酸除去铜中的铁.据此分析回答.
③考虑获取硫酸亚铁晶体的操作方法为结晶.
(2)①依据混合物分离的方法分析判断操作A,根据玻璃棒的应用分析其作用;
②由于目的是获得铜单质和硫酸亚铁,所以需要将铜离子转化为铜单质,而溶液中需要的是硫酸亚铁而不能引入新的杂质,所以加入的能够将铜离子转化为铜单质的只能是单质铁;由于加入的铁是过量的,需要加入过量稀硫酸除去铜中的铁.据此分析回答.
③考虑获取硫酸亚铁晶体的操作方法为结晶.
解答:解:
(1)由金属活动性顺序表的内容可知,介于Zn、Sn之间的是Fe;介于H、Hg之间的是Cu;介于Hg、Pt之间的是Ag.故填入下表如下:金属活动顺序表为:K Ca Na Mg Al,Zn Fe Sn Pb(H),Cu Hg Ag Pt Au;
(2)①过滤是将不溶性固体从溶液中分离出来的操作,所以由图示可知,该操作应该是过滤;组装过滤器需要的仪器有:烧杯、玻璃棒、铁架台、漏斗.故答:不溶;烧杯、玻璃棒、铁架台、漏斗;
②为回收废液中的Cu2+,需加入活动性在铜前面的金属进行置换,但要得到较为纯净FeSO4的溶液,只能向废液中加入过量的铁粉与硫酸铜发生置换反应,生成物中只有硫酸亚铁,加入其它金属溶液中又混有其它溶质.所以,金属X是Fe,其反应的化学方程式为:Fe+CuSO4=FeSO4+Cu;由于有过量铁粉,为除去混在铜粉里的铁粉并且得到FeSO4溶液,把金属混合物放入足量的稀硫酸并过滤即可.所以,溶液Y是H2SO4,其反应的化学方程式是:Fe+H2SO4=FeSO4+H2↑.
③要从滤液中获取硫酸亚铁晶体,需要采取蒸发结晶或降温结晶,使硫酸亚铁从溶液中结晶析出.故答:结晶(或蒸发结晶或冷却结晶).
故答案为:
(1)Na、Zn、Ag;(2)①不溶;烧杯、玻璃棒、铁架台、漏斗;
②Fe(或铁);Fe+CuSO4=FeSO4+Cu;稀硫酸;Fe+H2SO4=FeSO4+H2↑;③结晶(或蒸发结晶或冷却结晶)
(1)由金属活动性顺序表的内容可知,介于Zn、Sn之间的是Fe;介于H、Hg之间的是Cu;介于Hg、Pt之间的是Ag.故填入下表如下:金属活动顺序表为:K Ca Na Mg Al,Zn Fe Sn Pb(H),Cu Hg Ag Pt Au;
(2)①过滤是将不溶性固体从溶液中分离出来的操作,所以由图示可知,该操作应该是过滤;组装过滤器需要的仪器有:烧杯、玻璃棒、铁架台、漏斗.故答:不溶;烧杯、玻璃棒、铁架台、漏斗;
②为回收废液中的Cu2+,需加入活动性在铜前面的金属进行置换,但要得到较为纯净FeSO4的溶液,只能向废液中加入过量的铁粉与硫酸铜发生置换反应,生成物中只有硫酸亚铁,加入其它金属溶液中又混有其它溶质.所以,金属X是Fe,其反应的化学方程式为:Fe+CuSO4=FeSO4+Cu;由于有过量铁粉,为除去混在铜粉里的铁粉并且得到FeSO4溶液,把金属混合物放入足量的稀硫酸并过滤即可.所以,溶液Y是H2SO4,其反应的化学方程式是:Fe+H2SO4=FeSO4+H2↑.
③要从滤液中获取硫酸亚铁晶体,需要采取蒸发结晶或降温结晶,使硫酸亚铁从溶液中结晶析出.故答:结晶(或蒸发结晶或冷却结晶).
故答案为:
(1)Na、Zn、Ag;(2)①不溶;烧杯、玻璃棒、铁架台、漏斗;
②Fe(或铁);Fe+CuSO4=FeSO4+Cu;稀硫酸;Fe+H2SO4=FeSO4+H2↑;③结晶(或蒸发结晶或冷却结晶)
点评:本题考查了金属的活动性顺序的运用,首先明确金属和酸及金属和盐溶液反应的规律是解决问题的关键;然后根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,细致地阅读、分析题意等,联系着生活实际,细心地进行探究、推理,最后,按照题目的要求,进行解答即可.

练习册系列答案
相关题目
“藏独分子”在拉萨制造的纵火焚烧商店等事件,不仅影响国家安定团结,且给当地居民造成巨大损失.为最大程度保护居民的生命、财产安全,消防官兵立即前往火灾现场,并用高压水枪喷水灭火.水在灭火过程中的主要作用是( )
| A、降低可燃物的着火点 |
| B、防止燃烧产物污染环境 |
| C、吸收热量,降低燃烧环境的温度 |
| D、水分解出不助燃的物质 |
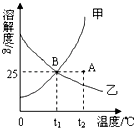 如图为甲、乙两种固体物质在水中的溶解度曲线:
如图为甲、乙两种固体物质在水中的溶解度曲线: 菠菜是一种营养价值很高的蔬菜.小明同学为了研究菠菜汁的成份,进行如下实验:
菠菜是一种营养价值很高的蔬菜.小明同学为了研究菠菜汁的成份,进行如下实验:
 根据如图简易电解水的装置回答问题:
根据如图简易电解水的装置回答问题: