题目内容
5.有一包固体,可能由硝酸铜、硫酸钠、氯化钠、碳酸钠、氢氧化钠中的一种或几种组成.为了探究该固体的组成,某化学小组设计并开展以下实验:已知,步骤Ⅰ中固体全部消失,溶液呈蓝色,无气泡产生.步骤Ⅱ、Ⅲ中均可观察到有白色沉淀生成.请回答下列问题:
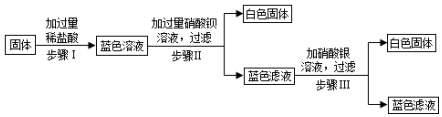
(1)原固体中一定含有的物质是硝酸铜、硫酸钠.
(2)原固体中一定不含有的物质是碳酸钠,证据是向固体中加过量稀盐酸,无气泡产生.
(3)步骤II中产生白色沉淀的化学方程式是Na2SO4+Ba(NO3)2═BaSO4↓+2NaNO3.
分析 根据固体加过量稀盐酸,固体完全溶解且溶液呈蓝色,说明固体中一定有硝酸铜;又因为无气泡产生,所以固体中一定不含有碳酸钠;步骤Ⅱ加入过量硝酸钡产生白色沉淀,说明固体中一定含有硫酸钠;步骤Ⅲ中加入硝酸银溶液,出现白色沉淀,则该白色沉淀为氯化银,由于一开始加入过量稀盐酸,所以溶液中一定有氯离子,所以会生成氯化银沉淀,但不能确定一定含有氯化钠进行分析.
解答 解:固体加过量稀盐酸,固体完全溶解且溶液呈蓝色,说明固体中一定有硝酸铜;又因为无气泡产生,所以固体中一定不含有碳酸钠;步骤Ⅱ加入过量硝酸钡产生白色沉淀,说明固体中一定含有硫酸钠;步骤Ⅲ中加入硝酸银溶液,出现白色沉淀,则该白色沉淀为氯化银,由于一开始加入过量稀盐酸,所以溶液中一定有氯离子,所以会生成氯化银沉淀,但不能确定一定含有氯化钠,所以
(1)根据分析可知:原固体中一定含有的物质是硝酸铜、硫酸钠;
(2)原固体中一定不含有的物质是碳酸钠,证据是:向固体中加过量稀盐酸,无气泡产生;
(3)步骤II中产生白色沉淀,即:硫酸钠溶液与硝酸钡溶液反应生成硫酸钡沉淀和硝酸钠,反应的化学方程式为:Na2SO4+Ba(NO3)2═BaSO4↓+2NaNO3.故答案为:
(1)硝酸铜、硫酸钠.
(2)碳酸钠,向固体中加过量稀盐酸,无气泡产生.
(3)Na2SO4+Ba(NO3)2═BaSO4↓+2NaNO3.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
15.已知氯气和氢氧化钠溶液反应的化学方程式:Cl2+2NaOH═NaCl+NaClO(次氯酸钠)+H2O,下列说法正确的是( )
| A. | 次氯酸钠中氯元素的化合价为-1 | |
| B. | 氯化钠中氯离子与次氯酸钠中的氯原子互为同位素 | |
| C. | 反应前氯气的质量和反应后溶液中氯元素的质量相等 | |
| D. | 氯化钠由钠元素和氯元素组成,所以为混合物 |
16. 有下列固体和液体组合:①锌粒和稀硫酸 ②双氧水和二氧化锰③氯化钠固体和水 ④生石灰和水要使图中的小气球鼓起来,固体和液体的组合可以是( )
有下列固体和液体组合:①锌粒和稀硫酸 ②双氧水和二氧化锰③氯化钠固体和水 ④生石灰和水要使图中的小气球鼓起来,固体和液体的组合可以是( )
 有下列固体和液体组合:①锌粒和稀硫酸 ②双氧水和二氧化锰③氯化钠固体和水 ④生石灰和水要使图中的小气球鼓起来,固体和液体的组合可以是( )
有下列固体和液体组合:①锌粒和稀硫酸 ②双氧水和二氧化锰③氯化钠固体和水 ④生石灰和水要使图中的小气球鼓起来,固体和液体的组合可以是( )| A. | ①②③④ | B. | ①②④ | C. | ①③④ | D. | ①②③ |
20.化学工业给社会带来巨大财富和众多产品的同时,也带来了环境问题.在化学工业中除了要及时处理好“三废”,还要努力提高原料的利用率,增加产品的产量,降低生产对环境造成的污染,符合“绿色化学”.以铜等原料制取氢氧化铜,下列方案中,“符合绿色化学”的是( )
| A. | Cu$\stackrel{+HCl}{→}$CuCl2$\stackrel{+KOH}{→}$Cu(OH)2 | |
| B. | Cu$\stackrel{+O_{2}}{→}$CuO$\stackrel{+H_{2}SO_{4}}{→}$CuSO4$\stackrel{+NaOH}{→}$Cu(OH)2 | |
| C. | Cu$\stackrel{+O_{2}}{→}$CuO$\stackrel{+H_{2}SO_{4}}{→}$CuSO4$\stackrel{+Ba(OH)_{2}}{→}$Cu(OH)2 | |
| D. | Cu$\stackrel{+H_{2}SO_{4}(浓)}{→}$CuSO4$\stackrel{+NaOH}{→}$Cu(OH)2 |
10.某城市有甲、乙两工厂排放污水,污水中各含有下列6种离子中的3种(两厂不含相同离子):H+、Ba2+、Na+、OH-、CO32-、NO3-.两厂单独排放都会造成严重的水污染,若将两厂的污水按一定比例混合,便会变成无色澄清只含硝酸钠的溶液.关于污染源的分析,你认为正确的是( )
| A. | CO32- 和NO3- 来自同一工厂 | B. | OH-和NO3- 一定不在同一工厂 | ||
| C. | H+和Ba2+一定不在同一工厂 | D. | Na+和NO3- 来自同一工厂 |
14.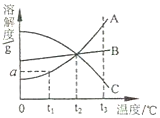 如图是 A、B、C 三种固体物质(均不含结晶水)的溶解度曲线,根据图示,下列说法 不正确的是( )
如图是 A、B、C 三种固体物质(均不含结晶水)的溶解度曲线,根据图示,下列说法 不正确的是( )
 如图是 A、B、C 三种固体物质(均不含结晶水)的溶解度曲线,根据图示,下列说法 不正确的是( )
如图是 A、B、C 三种固体物质(均不含结晶水)的溶解度曲线,根据图示,下列说法 不正确的是( )| A. | t1℃时,取 50gA 的饱和溶液,将温度升高到 t2℃,此时溶液中 A 的质量分数变大(假设升温时溶剂没有损失) | |
| B. | t1℃,将 A、B、C 各 ag放入100g水中,充分搅拌,所得溶液溶质质量分数均相等 | |
| C. | t3℃时,取相同质量的A、B、C三种饱和溶液降温到 t1℃析出晶体最多的是A,没有晶体析出并变成不饱和溶液的是C | |
| D. | 从 A与少量C的混合物中提纯A,可用降温结晶的方法 |

 市售的碳酸氢钠片是一种白色片状药剂,主要成份为碳酸氢钠(NaHCO3),用于缓解胃酸过多引起的胃痛、胃灼热感(烧心)、反酸等有关症状,根据题意,试回答以下问题:
市售的碳酸氢钠片是一种白色片状药剂,主要成份为碳酸氢钠(NaHCO3),用于缓解胃酸过多引起的胃痛、胃灼热感(烧心)、反酸等有关症状,根据题意,试回答以下问题: