题目内容
8.(1)2015年4月25日世兵赛在苏州隆重举行,运动员在开赛前可以适当补充些葡萄糖,供给能量,若血液中缺乏葡萄糖则可能引起低血糖疾病.在淀粉酶的催化作用下,谷类食品中所含的淀粉[(C6H10O5)n]能与水反应,生成易溶于水的葡萄糖(C6H12O6).请你写出相应的化学方程式:(C6H10O5)n+nH2O$\frac{\underline{\;淀粉酶\;}}{\;}$nC6H12O6.(2)从下列仪器和药品中选用①②或⑤⑥两种组合方法(填序号,可重复使用),探究“某无色液体是蒸馏水还是葡萄糖溶液”.
①酒精灯 ②试管及试管夹 ③玻璃棒 ④碘水 ⑤硫酸铜溶液 ⑥氢氧化钠溶液
(3)计算溶质质量分数为10%的葡萄糖溶液中氢元素的质量分数(写出计算过程,结果保留到0.1%)
分析 (1)根据若血液中缺乏葡萄糖则可能引起低血糖疾病、淀粉[(C6H10O5)n]能与水反应生成葡萄糖进行解答;
(2)检验葡萄糖用新制的氢氧化铜悬浊液,可取样与新制的氢氧化铜悬浊液共热,若有砖红色的氧化亚铜沉淀生成,说明是葡萄糖溶液,据此进行分析解答.
(3)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;葡萄水属于碳水化合物,其中H、O元素质量比与水中H、O元素质量相同,据此可判断溶液中H、O元素质量比,可完成溶液中H元素质量分数的计算.
解答 解:(1)若血液中缺乏葡萄糖则可能引起低血糖疾病;淀粉[(C6H10O5)n]能与水反应生成葡萄糖,相应的化学方程式:(C6H10O5)n+nH2O$\frac{\underline{\;淀粉酶\;}}{\;}$nC6H12O6;
故填:低血糖;(C6H10O5)n+nH2O$\frac{\underline{\;淀粉酶\;}}{\;}$nC6H12O6;
(2)检验葡萄糖用新制的氢氧化铜悬浊液,取样与新制的氢氧化铜悬浊液共热,若有砖红色的氧化亚铜沉淀生成,说明是葡萄糖溶液,若无明显变化,说明是蒸馏水;制取氢氧化铜沉淀选用硫酸铜溶液和氢氧化钠溶液;取样与新制的氢氧化铜悬浊液共热,选用酒精灯和试管、试管夹.
故选用的仪器和药品的组合是①②和⑤⑥.故填:①②,⑤⑥;
(3)因为葡萄糖的化学式为C6H12O6,故其氢、氧元素的质量比=(1×12):(16×6)=1:8,其相对分子质量为12×6+1×12+16×6=180;故该葡萄糖的水溶液内氢、氧元素的质量比为1:8;根据“溶质质量分数为10%的葡萄糖溶液”,设溶液的质量为100g,则葡萄糖的质量为10g,则其中氢元素的质量分数为:$(1-\frac{10g×\frac{12×6}{180}}{100g})×100%×\frac{1}{1+8}≈10.7%$;故填:10.7%.
点评 本题考查了化学方程式的书写、葡萄糖的检验以及溶液中国某元素的质量分数的计算,本题的巧妙之处在于葡萄糖溶液中因为葡萄糖和水中H、O元素质量比均为1:8,从而可判断由这两种物质形成的混合物中H、O质量比也为1:8.

| A. | 控制二氧化碳、臭氧、甲烷、氟氯代烷等气体的排放,能减缓温室效应 | |
| B. | 煤、汽油等燃料充分燃烧对于节约能源,减少环境污染非常重要 | |
| C. | 不合理使用农药会造成对自然环境的污染,但不会危害人体健康 | |
| D. | 难于降解的废弃塑料产生“白色污染”,回收废弃塑料,可解决白色污染问题 |
 许多化学反应都伴随着明显的现象的发生,但也有一些观察不到明显的现象.如将二氧化碳通入澄清石灰水中,溶液变浑浊;但将二氧化碳通入氢氧化钠溶液中,却无明显现象.
许多化学反应都伴随着明显的现象的发生,但也有一些观察不到明显的现象.如将二氧化碳通入澄清石灰水中,溶液变浑浊;但将二氧化碳通入氢氧化钠溶液中,却无明显现象.【提出问题】二氧化碳通入氢氧化钠溶液中无明显现象,两者是否发生了化学反应?
【猜想假设】猜想①:两者发生了化学反应;猜想②:两者没有发生化学反应
【实验探究】
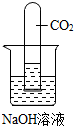
(1)甲同学设计了如图实验:把一支收集有CO2的试管倒立在装有饱和NaOH溶液的烧杯中,看到试管内出现了液面升高现象.乙同学认为甲同学的实验是可行的,其原理是二氧化碳和氢氧化钠溶液反应,使试管内压强降低.但丙同学和丁同学却对此提出质疑,他们认为甲的实验不严谨,其理由是二氧化碳能与水反应或溶于水,也能使容器内气体减少,压强减小.
(2)为了进一步证实CO2与NaOH溶液是否发生了反应,丙同学和丁同学分别加入两类不同的物质,通过检验生成物的实验方案,请你填写下面实验报告:
| 实验操作 | 实验现象 | 化学反应方程式 | 实验结论 | |
| 取上述实验 后的溶液 | 丙同学滴加稀盐酸 | 有气泡产生 | 2HCl+Na2CO3=2NaCl+H2O+CO2↑ | 验证了二氧化碳与氢氧化钠的反应 |
| 丁同学滴加氯化钙 | 生成白色沉淀 | CaCl2+Na2CO3=CaCO3↓+2NaCl | ||
【反思】对于没有明显现象的化学反应,可以从两个不同的角度证明反应的发生,一是可以通过检验生成物证明反应发生;二是可以通过检验反应物减少证明反应发生.
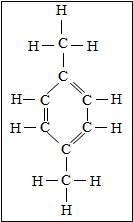 清华大学化工系学生发起一场PX词条“保卫战”,经过多次“拉锯”修改,2014年4月4日,百度百科上“PX”词条最终被锁定在“低毒化合物”的准确描述上.PX是对二甲苯,其组成和结构如图所示:下列有关说法正确的是( )
清华大学化工系学生发起一场PX词条“保卫战”,经过多次“拉锯”修改,2014年4月4日,百度百科上“PX”词条最终被锁定在“低毒化合物”的准确描述上.PX是对二甲苯,其组成和结构如图所示:下列有关说法正确的是( )| A. | 对二甲苯中的C、H元素的质量比为48:5 | |
| B. | 对二甲苯分子是由6个碳元素和6个氢元素组成 | |
| C. | 对二甲苯分子中碳的原子结构示意图为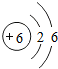 | |
| D. | 对二甲苯中碳、氢元素均位于元素周期表的第二周期 |
| A. | 用水壶烧水时,壶盖被顶开,说明水分子的体积在受热时变大了 | |
| B. | 水可以结成冰,说明水分子的化学性质发生改变 | |
| C. | 电解水生成氢气与氧气,说明水分子可以再分解 | |
| D. | 发生化学反应时,构成水分子的原子种类发生改变 |
| A. | +6 | B. | +3 | C. | +4 | D. | +2 |