题目内容
17. 在做盐跟盐反应的分组实验时,第一组学生进行BaCl2与Na2CO3溶液的反应,第二组学生进行BaCl2与Na2SO4溶液的反应.实验结束后,两组同学将全部的浊液集中倒进一个废液缸中.浊液中白色沉淀物质是碳酸钡和硫酸钡.
在做盐跟盐反应的分组实验时,第一组学生进行BaCl2与Na2CO3溶液的反应,第二组学生进行BaCl2与Na2SO4溶液的反应.实验结束后,两组同学将全部的浊液集中倒进一个废液缸中.浊液中白色沉淀物质是碳酸钡和硫酸钡.化学兴趣小组对浊液进行过滤,探究滤液的成分.
【提出问题】滤液里除了NaCl外,还有什么物质?
【提出猜想】猜想①:BaCl2; 猜想②:Na2SO4;
猜想③:Na2CO3; 猜想④:Na2CO3、Na2SO4
【实验探究】
若现象a只有白色沉淀,则猜想①成立,则生成沉淀的反应方程式为BaCl2+Na2SO4═BaSO4↓+2NaCl;若现象a只有气泡产生,则猜想③④可能成立,则生成气体的反应方程式为Na2CO3+H2SO4=Na2SO4+H2O+CO2↑;若现象b产生白色沉淀,然后加稀硝酸沉淀部分溶解,并产生气泡,则猜想④成立,若沉淀全部不溶解,则猜想②成立.
分析 氯化钡和碳酸钠反应能够生成碳酸钡沉淀和氯化钠,和硫酸钠反应能够生成硫酸钡沉淀和氯化钠;
当氯化钡过量时,滤液中含有氯化钠和氯化钡;当碳酸钠过量时,滤液中含有氯化钠和碳酸钠;当硫酸钠过量时,滤液中含有硫酸钠;当碳酸钠、硫酸钠都过量时,滤液中含有氯化钠、碳酸钠和硫酸钠;根据实验现象可以判断滤液中溶质的存在情况.
解答 解:氯化钡和碳酸钠反应能够生成碳酸钡沉淀和氯化钠,和硫酸钠反应能够生成硫酸钡沉淀和氯化钠,浊液中白色沉淀物质是碳酸钡和硫酸钡.
故填:碳酸钡;硫酸钡.
[提出猜想]
当氯化钡过量时,滤液中含有氯化钠和氯化钡;当碳酸钠过量时,滤液中含有氯化钠和碳酸钠;当硫酸钠过量时,滤液中含有硫酸钠;当碳酸钠、硫酸钠都过量时,滤液中含有氯化钠、碳酸钠和硫酸钠,滤液里除了NaCl外,还可能含有氯化钡,或硫酸钠,或碳酸钠,或碳酸钠和硫酸钠.
故填:BaCl2.
[实验探究]
若现象a只有白色沉淀,则滤液中含有氯化钠和氯化钡,因为氯化钡与硫酸反应生成硫酸钡沉淀和氯化氢.反应的化学方程式为:BaCl2+Na2SO4═BaSO4↓+2NaCl.
故填:①.BaCl2+Na2SO4═BaSO4↓+2NaCl.
若现象a只有气泡产生,则滤液中含有氯化钠和碳酸钠,或含有氯化钠、碳酸钠和硫酸钠.
故填:③④.
稀硫酸和碳酸钠反应能够生成氯化钠、水和二氧化碳,化学方程式为:
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑.
故填:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑.
若现象b产生白色沉淀,然后加稀硝酸沉淀部分溶解,并产生气泡,说明滤液中含有氯化钠、碳酸钠和硫酸钠,因为氯化钡和碳酸钠反应生成的碳酸钡沉淀能够和稀硝酸反应,而氯化钡和硫酸钠反应生成的硫酸钡不能和稀硝酸反应.
故填:④.
若沉淀全部不溶解,则滤液中含有氯化钠和硫酸钠.
故填:②.
点评 实验现象明显、直观,可以帮助我们更好地理解反应过程,因此要注意观察实验现象,学会分析实验现象,从而进行正确的判断.

 如图为检查装置气密性的实验,夏天温度高,手握试管很难观察到导管出口冒气泡的现象,可以另外采取多种措施进行检验,以下措施不能采纳的是( )
如图为检查装置气密性的实验,夏天温度高,手握试管很难观察到导管出口冒气泡的现象,可以另外采取多种措施进行检验,以下措施不能采纳的是( )| A. | 将试管浸在冰水中 | B. | 用热毛巾捂住试管 | ||
| C. | 对着试管壁持续哈气 | D. | 用酒精灯微热试管 |
| A. | 矿泉水 | B. | 河水 | C. | 五氧化二磷 | D. | 水泥沙浆 |
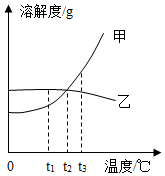 t3℃时,两个烧杯中分别盛有甲、乙两种物质的恰好饱和溶液.甲乙两种物质的溶解度曲线如图所示.下列说法正确的是( )
t3℃时,两个烧杯中分别盛有甲、乙两种物质的恰好饱和溶液.甲乙两种物质的溶解度曲线如图所示.下列说法正确的是( )| A. | t1℃,两烧杯溶液中的溶质的质量一定相同 | |
| B. | 升高温度,甲杯的固体不断增大,乙杯的固体不断减少 | |
| C. | 降低温度的过程中,两烧杯中溶液的溶质质量分数可能相等 | |
| D. | 从甲乙的混合物中分离得到甲可以采用蒸发溶剂的方法 |
| A. | Na Mg Cu | B. | CH4 C2H5OH C6H12O6 | ||
| C. | NaCl AgNO3 BaSO4 | D. | NaOH H2SO4 空气 |
 缺钙会导致儿童发育不良或佝偻病.小明同学从食物中摄入钙元素的量不足,每天需要服用2片某种钙片.该钙片标签的部分内容如图所示(假设钙片中只有碳酸钙含有钙元素),请计算:
缺钙会导致儿童发育不良或佝偻病.小明同学从食物中摄入钙元素的量不足,每天需要服用2片某种钙片.该钙片标签的部分内容如图所示(假设钙片中只有碳酸钙含有钙元素),请计算: