题目内容
7.下列物质的用途是由其化学性质决定的是( )| A. | 干冰做制冷剂 | B. | 石墨做电极 | ||
| C. | 铁制成铁锅 | D. | 氮气用于食品防腐 |
分析 物质在化学变化中表现出来的性质叫化学性质,物质不需要发生化学变化就表现出来的性质,叫物理性质;物理性质经常表现为:颜色、状态、气味、密度、硬度、熔点、沸点、导电性、导热性、溶解性、挥发性等.
解答 解:A、干冰做制冷剂是利用干冰升华吸热,属于物理性质,故选项错误;
B、石墨做电极是利用石墨的导电性,属于物理性质,故选项错误;
C、铁制成铁锅是利用铁的导热性,属于物理性质,故选项错误;
D、氮气用于食品防腐是利用氮气的化学性质稳定,故选项正确;
故选D
点评 本考点考查了物理性质和化学性质的区分,要记忆有关物质的性质,并能够在比较的基础上进行应用,本考点的基础性比较强,主要出现在选择题和填空题中.

练习册系列答案
相关题目
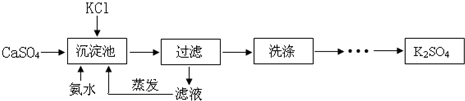
17.以硫酸钙晶体(石膏的主要成分)与氯化钾为原料制备硫酸钾的流程如图:
已知硫酸钾在不同温度下在水溶液、氨溶液中的溶解度(g)
(1)氨水显碱性(填“酸性”、“碱性”或“中性”),向水中连续通氨气达两个小时可得高浓度氨水,氨气不断溶解使溶液pH增大(填“增大”、“减小”或“不变”).上表中“非常压”指需增大气压才能形成30℃的氨(35%)溶液,常压下不能形成30℃的氨(35%)溶液的原因是常压30℃时氨气在水中达到饱和时浓度小于35%.
(2)沉淀池中氨水浓度常常控制在25%至40%,其原因是氨水浓度越大,硫酸钾溶解度越小,沉淀池温度适宜保持
低温(选填“低温”或“高温”).
(3)滤液经蒸发后产生可以循环使用的气体,其化学式为NH3;滤液中的副产品氯化钙可转化成碳酸钙固体,与HNO3反应制备Ca(NO3)2•6H2O晶体,为确保制备过程中既不补充水,也无多余的水,所用硝酸溶液中溶质与溶剂的质量比为7:5.
(4)实验室进行过滤操作需要的玻璃仪器有烧杯、玻璃棒、漏斗,其中玻璃棒在稀释浓硫酸时也用到,稀释浓硫酸时用到玻璃棒的主要作用为使溶解产生的热量及时散发,防止局部过热而引起液体飞溅.
(5)检验沉淀是否洗净的试剂是AB(填序号)
A.酚酞试液 B碳酸钠溶液 C氯化钡溶液
(6)烟气脱硫能有效减少二氧化硫的排放,能将其转化为石膏(CaSO4•2H2O)等产品,实现“变废为宝”.二氧化硫的排放会导致的环境问题是形成酸雨,可用高锰酸钾溶液检验烟气中二氧化硫.
(7)某电厂用煤200吨(含硫质量分数为2.5%),若燃烧时煤中的硫全部转化成二氧化硫,烟气脱硫中有96%的硫转化为石膏(CaSO4•2H2O),则可生产石膏多少吨?

已知硫酸钾在不同温度下在水溶液、氨溶液中的溶解度(g)
| 温度(℃) | 0 | 10 | 26 | 30 |
| 水溶液 | 7.31 | 9.28 | 11.03 | 12.98 |
| 氨(8%)溶液 | 1.41 | 1.58 | 2.25 | 3.36 |
| 氨(35%)溶液 | 0.44 | 0.75 | 0.82 | 非常压 |
(2)沉淀池中氨水浓度常常控制在25%至40%,其原因是氨水浓度越大,硫酸钾溶解度越小,沉淀池温度适宜保持
低温(选填“低温”或“高温”).
(3)滤液经蒸发后产生可以循环使用的气体,其化学式为NH3;滤液中的副产品氯化钙可转化成碳酸钙固体,与HNO3反应制备Ca(NO3)2•6H2O晶体,为确保制备过程中既不补充水,也无多余的水,所用硝酸溶液中溶质与溶剂的质量比为7:5.
(4)实验室进行过滤操作需要的玻璃仪器有烧杯、玻璃棒、漏斗,其中玻璃棒在稀释浓硫酸时也用到,稀释浓硫酸时用到玻璃棒的主要作用为使溶解产生的热量及时散发,防止局部过热而引起液体飞溅.
(5)检验沉淀是否洗净的试剂是AB(填序号)
A.酚酞试液 B碳酸钠溶液 C氯化钡溶液
(6)烟气脱硫能有效减少二氧化硫的排放,能将其转化为石膏(CaSO4•2H2O)等产品,实现“变废为宝”.二氧化硫的排放会导致的环境问题是形成酸雨,可用高锰酸钾溶液检验烟气中二氧化硫.
(7)某电厂用煤200吨(含硫质量分数为2.5%),若燃烧时煤中的硫全部转化成二氧化硫,烟气脱硫中有96%的硫转化为石膏(CaSO4•2H2O),则可生产石膏多少吨?
18.下列自然资源的利用过程中,发生了化学变化的是( )
| A. | 风力发电 | B. | 木材制桌椅 | C. | 海水晒盐 | D. | 木柴燃烧 |
15. 将一定质量的Ca(OH)2溶液与Na2CO3溶液混合恰好完全反应,向反应后的混合物中加入稀盐酸,产生气体的体积与加入稀盐酸的体积的关系如图所示,下列说法中正确的是( )
将一定质量的Ca(OH)2溶液与Na2CO3溶液混合恰好完全反应,向反应后的混合物中加入稀盐酸,产生气体的体积与加入稀盐酸的体积的关系如图所示,下列说法中正确的是( )
 将一定质量的Ca(OH)2溶液与Na2CO3溶液混合恰好完全反应,向反应后的混合物中加入稀盐酸,产生气体的体积与加入稀盐酸的体积的关系如图所示,下列说法中正确的是( )
将一定质量的Ca(OH)2溶液与Na2CO3溶液混合恰好完全反应,向反应后的混合物中加入稀盐酸,产生气体的体积与加入稀盐酸的体积的关系如图所示,下列说法中正确的是( )| A. | N点时,所得溶液中的溶质只有NaCl和HCl | |
| B. | M点时,所得溶液的pH>7 | |
| C. | OP段发生反应的化学方程式为Ca(OH)2+2HCl=CaCl2+2H2O | |
| D. | PM段发生反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑ |
 如图所示是被称之为“软电池”的纸质电池,采用薄层纸片作为传导体,在其一边镀锌,可作为电池负极,另一边镀二氧化锰作为电池正极.电池总反应为:Zn+2MnO2+H2O=ZnO+2MnO(OH).
如图所示是被称之为“软电池”的纸质电池,采用薄层纸片作为传导体,在其一边镀锌,可作为电池负极,另一边镀二氧化锰作为电池正极.电池总反应为:Zn+2MnO2+H2O=ZnO+2MnO(OH).
 在测定空气中氧气含量的实验中,小强采用了右图所示装置:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的玻璃管加热,同时缓慢推动两个注射器活塞,至玻璃管内的铜丝在较长时间内无进一步变化时停止加热,待冷却至室温,将气体全部推至一个注射器内,观察密闭系统内空气体积变化.
在测定空气中氧气含量的实验中,小强采用了右图所示装置:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的玻璃管加热,同时缓慢推动两个注射器活塞,至玻璃管内的铜丝在较长时间内无进一步变化时停止加热,待冷却至室温,将气体全部推至一个注射器内,观察密闭系统内空气体积变化.