题目内容
4.6g某物质在空气中完全燃烧生成8.8g二氧化碳和5.4g水,则关于这种物质的组成描述正确的是( )
| A、该物质一定只含有碳、氢两种元素 |
| B、该物质一定含有碳、氢、氧三种元素 |
| C、该物质一定含有碳、氢两种元素,可能含有氧元素 |
| D、以上答案均不正确 |
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:化学反应遵循质量守恒定律,即参加反应的物质的质量之和,等于反应后生成的物质的质量之和; 化学反应前后,元素的种类不变,原子的种类、总个数不变.
解答:解:8.8g二氧化碳中碳元素的质量为:8.8g×
×100%=2.4g;5.4g水中氢元素的质量为:5.4g×
×100%=0.6g;
该物质中氧元素的质量为:4.6g-2.4g-0.6g=1.6g;
二氧化碳中的碳元素和水中的氢元素来自于该物质,因此该物质一定含有碳、氢、氧三种元素.
故选:B.
| 12 |
| 44 |
| 2 |
| 18 |
该物质中氧元素的质量为:4.6g-2.4g-0.6g=1.6g;
二氧化碳中的碳元素和水中的氢元素来自于该物质,因此该物质一定含有碳、氢、氧三种元素.
故选:B.
点评:化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.

练习册系列答案
相关题目
下列自救措施中不合理的是( )
| A、室内起火不要急于打开所有门窗 |
| B、厨房煤气泄漏,不要立即打开抽油烟机 |
| C、火灾发生且烟雾较浓时,用湿毛巾捂住口鼻,迅速逃离 |
| D、在山林中遇到火灾时,向顺风方向奔跑,逃离火灾区 |
科学实验测定,正确情况下,人类头发的化学组成为:碳45%,氧28%,氮15%,氢7%,硫5%,则焚烧头发不可能生成的物质是( )
| A、H2O |
| B、CO2 |
| C、SO2 |
| D、HCl |
化学方程式为:C+2H2SO4(浓)
X↑+2SO2↑+2H2O,则X的化学式是( )
| ||
| A、CO2 |
| B、CO |
| C、SO3 |
| D、H2SO4 |
下列变化属于化学变化的是( )
| A、洗涤剂清洗油污 | B、酒精挥发 |
| C、干冰升华 | D、食物腐败 |

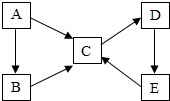 A、B、C、D、E均为初中化学常见物质,他们之间转化关系如图所示:(“→”表示某一种物质经一步反应可转化为另一种物质,部分生成物及反应条件已略去)
A、B、C、D、E均为初中化学常见物质,他们之间转化关系如图所示:(“→”表示某一种物质经一步反应可转化为另一种物质,部分生成物及反应条件已略去)