题目内容
6.实验室配制500g溶质的质量分数为10%的NaCl溶液.如图是配制过程的示意图: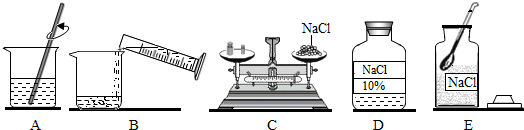
①图中有一项C(填字母)操作有明显错误.
②纠正错误后,配制溶液的正确操作顺序为E、C、B、A、D.
③要配制200g 0.9%的生理盐水(NaCl溶液),需10%的NaCl溶液18g,并加水稀释.
分析 (1)根据托盘天平的使用要遵循“左物右码”的原则,进行分析解答.
(2)根据配制溶质质量分数一定的溶液的基本步骤进行分析解答.
(3)根据溶液稀释前后,溶质的质量不变,结合题意进行分析解答.
解答 解:(1)托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了,所示操作错误.
(2)配制500g溶质的质量分数为10%的NaCl溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解,故纠正错误后,配制溶液的正确操作顺序为E、C、B、A、D.
(3)要配制200g 0.9%的生理盐水(NaCl溶液),设需10%的NaCl溶液的质量为x,根据溶液稀释前后,溶质的质量不变,则200g×0.9%=x×10% x=18g.
故答案为:(1)C;(2)C、B、A;(3)18.
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、注意事项、溶液稀释前后溶质的质量不变是正确解答本题的关键.

练习册系列答案
 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
16.“催化转化器”可以将汽车尾气中有害气体处理为无污染的气体,如图为该反应的微观示意图,其中不同颜色的球代表不同的原子.下列说法正确的是( )
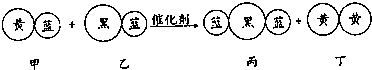
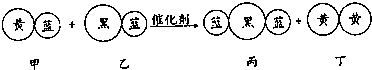
| A. | 乙和丙中所含的元素种类不同 | B. | 甲和丁中同种元素的化合价相等 | ||
| C. | 该反应中共有三种元素 | D. | 乙和丁都是化合物 |
11.把O2,CO2,N2,Cl2关在一个房子里,(假设房子里无任何气体,且绝对密闭),然后打开房顶的烟囱,谁能够先全身而退( )
| A. | O2 | B. | CO2 | C. | N2 | D. | Cl2 |
18.海水是资源的宝库,海水淡化可获得淡水和浓海水.浓海水中主要离子的浓度如下:
从浓海水中提取金属镁的一段工艺流程如图所示:
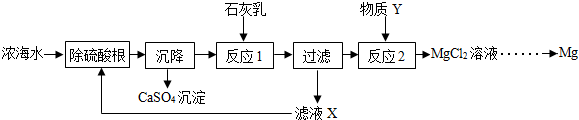
(1)补全由贝壳生产石灰乳的相应转化中所需的条件或反应物:
贝壳$\stackrel{()}{→}$生石灰$\stackrel{()}{→}$石灰乳
(2)写出反应1的化学方程式:Ca(OH)2+MgCl2=CaCl2+Mg(OH)2↓.
(3)滤液X中溶质的主要成分有CaCl2、NaCl(填化学式).
(4)物质Y的名称是盐酸.
(5)将MgCl2溶液在一定条件下蒸发结晶、熔融电解可制得金属镁.则2L浓海水理论上可得到金属镁的质量为57.6g.
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/g/L | 63.7 | 28.8 | 144.6 | 46.4 |

(1)补全由贝壳生产石灰乳的相应转化中所需的条件或反应物:
贝壳$\stackrel{()}{→}$生石灰$\stackrel{()}{→}$石灰乳
(2)写出反应1的化学方程式:Ca(OH)2+MgCl2=CaCl2+Mg(OH)2↓.
(3)滤液X中溶质的主要成分有CaCl2、NaCl(填化学式).
(4)物质Y的名称是盐酸.
(5)将MgCl2溶液在一定条件下蒸发结晶、熔融电解可制得金属镁.则2L浓海水理论上可得到金属镁的质量为57.6g.
16.生活中处处有化学,下列说法错误的是( )
| A. | 医疗上常用体积分数为70%的酒精作消毒剂 | |
| B. | 长期过量摄入食盐,会引起高血压等病症 | |
| C. | 汽车安装尾气净化装置,以节约石油资源 | |
| D. | 经常使用染发剂,不利于身体健康 |