题目内容
Na2SO4和CaSO4组成的混合物中,测知氧元素的质量分数为46%.若再计算混合物中的下列各项:①硫元素的质量分数 ②钠元素的质量分数 ③CaSO4的质量分数 ④Na2SO4和CaSO4的质量比 ⑤CaSO4的质量,以下判断正确的是
A.都能确定 B.都不能确定 C.只有①能确定 D.只有⑤不能确定
D

下图所示为实验室中常见的气体制备和收集装置。请回答下列问题:
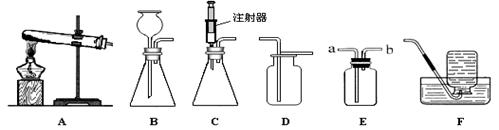 |
(1)请写出一个实验室用A装置制取氧气的化学方程式___________ ___________。(2分)
___________。(2分)
(2)用过氧化氢溶液和二氧化锰制氧气,用C做发生装置的优点是_________________。
(3)装置E用排空气法收集氧气,则气体应从 (填“a”或“b”)端通入;欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从 端通入。
(4)常温下,硫化氢(H2S)是一种有臭鸡蛋气味的气体,实验室可用硫化亚铁(FeS)固体和稀硫酸常温反应制得,则应选择 (填序号)来作发生装置。
 (5)实验室常用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,发生装置可选择__________(填序号)。甲烷气体一般采用装置F进行收集,收集满后集气瓶的放置方式如右图所示,据此可推断甲烷一定具备的物理性质是:___________、__________________。
(5)实验室常用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,发生装置可选择__________(填序号)。甲烷气体一般采用装置F进行收集,收集满后集气瓶的放置方式如右图所示,据此可推断甲烷一定具备的物理性质是:___________、__________________。
(6)装置的气密性是保证气体实验成功的关键,下列图示操作中,能用于检查气密性的是_______________ ______。(2分)
______。(2分)
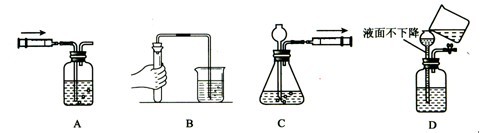
下列实验操作正确的是( )
|
| A. |
液体读数 | B. |
液体取用 | C. |
过滤 | D. |
滴加液体 |
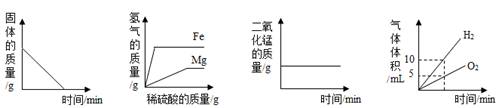
下列四个坐标示意图分别表示四个实验过程中的某些变化情况,其中错误的是
|
A.加热一定量碳铵(NH4HCO4)的实验,试管中固体的质量变化
B .等质量的镁条和铁丝分别与足量的稀硫酸反应,产生气体的质量变化
.等质量的镁条和铁丝分别与足量的稀硫酸反应,产生气体的质量变化
C.向一定量的二氧化锰固体中加入一定量的过氧化氢溶液,二氧化锰的质量变化
D.将水通电一段时间,相同状况下产生气体的体积变化
与元素化学性质的关系最密切的是( )
|
| A. | 元素的相对原子质量 | B. | 原子核内的中子数 |
|
| C. | 原子核内的质子数 | D. | 原子核外的最外层电子数 |
小明发现一种淡黄色的粉末可以用于杀菌、消毒和漂白,于是想探究该固体的成分.
【提出问题】该淡黄色固体的化学成分是什么?
【查阅资料】
(1)硫单质是一种淡黄色固体,难溶于水,在空气中点燃硫单质,生成一种无色、有刺激性气味的气体.
(2)过氧化钠(Na2O2)是一种淡黄色固体,能与水反应,生成气体并放出大量的热.
【设计实验方案】
方案一:取少量该固体粉末于试管中,加2mL水,振荡并观察现象.
方案二:在燃烧匙里放少量该固体,在酒精灯上加热,观察现象.
比较以上两方案,你认为的最佳方案是 ,理由是(从环保、操作等角度分析) .
【实验验证并得出结论】
小明向盛有少量该固体的试管中加入2mL水,立刻观察到有无色气泡产生,并且验证出该反应同时生成了氢氧化钠(NaOH).通过实验验证,确定该淡黄色粉末为过氧化钠.
小明想对生成的气体成分判断,他提出了以下两种假设:①该气体是CO ②该气体是O2
你认为上述假设哪个更合理 ② (填“①”或“②”).
请设计一个实验,验证你的合理假设(写出简要操作步骤、实验现象和结论).
| 操作步骤 | 实验现象 | 结论 |
|
|
|
|
【分析】过氧化钠与水反应的文字表达式为 .
【计算】在过氧化钠(Na2O2)中,
①氧元素的化合价为 ;
②过氧化钠的相对分子质量为 ;
③过氧化钠中钠、氧元素的质量比为 ;
④78克过氧化钠与多少克二氧化碳中所含氧元素的质量相等?(列式计算)



 : ;水和双氧水都含有相同的元素,但化学性质不同,原因是 。
: ;水和双氧水都含有相同的元素,但化学性质不同,原因是 。 (4)在生产生活中水是最常用的溶剂,实验室用蔗糖配制一定溶质质量分数的溶液时,可能涉及以下操作:
(4)在生产生活中水是最常用的溶剂,实验室用蔗糖配制一定溶质质量分数的溶液时,可能涉及以下操作: 溶液方法有 、 。(写出两种)
溶液方法有 、 。(写出两种)