题目内容
为了测定某样品中氧化铁(Fe2O3)的质量分数(杂质不含铁元素,且不溶于水和酸),某兴趣小组的同学进行了如下的实验,请你参与过程分析.
【查阅资料】
1.草酸(H2C2O4)在浓硫酸作用下受热分解,化学方程式为H2C2O4
CO2↑+CO↑+H2O;
2.碱石灰主要成分为生石灰与氢氧化钠固体.
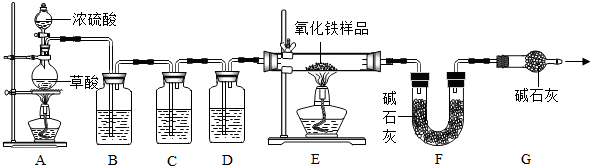
【实验设计及操作】用如图所示装置进行实验.
【问题讨论】
(1)实验中观察到E中现象是 ;
(2)进入E中的气体是纯净、干燥的CO,则B、C、D中依次是 (填序号);
①浓硫酸、石灰水、氢氧化钠溶液
②石灰水、氢氧化钠溶液、浓硫酸
③氢氧化钠溶液、石灰水、浓硫酸
(3)当E中固体完全反应后,先熄灭 处酒精灯(填“A”或“E”);
(4)G的作用是 ;
(5)实验装置有一明显缺陷是 .
【数据处理】称取样品8.0g,用上述装置进行实验,充分反应后称量F装置增重4.4g.则样品中氧化铁质量分数为 (精确到0.1%).
【实验反思】当观察到E中固体全部变黑后,若立即停止通CO,则测得的样品中氧化铁的质量分数 (填“偏大”、“偏小”或“无影响”).

【查阅资料】
1.草酸(H2C2O4)在浓硫酸作用下受热分解,化学方程式为H2C2O4
| ||
| △ |
2.碱石灰主要成分为生石灰与氢氧化钠固体.
【实验设计及操作】用如图所示装置进行实验.
【问题讨论】
(1)实验中观察到E中现象是
(2)进入E中的气体是纯净、干燥的CO,则B、C、D中依次是
①浓硫酸、石灰水、氢氧化钠溶液
②石灰水、氢氧化钠溶液、浓硫酸
③氢氧化钠溶液、石灰水、浓硫酸
(3)当E中固体完全反应后,先熄灭
(4)G的作用是
(5)实验装置有一明显缺陷是
【数据处理】称取样品8.0g,用上述装置进行实验,充分反应后称量F装置增重4.4g.则样品中氧化铁质量分数为
【实验反思】当观察到E中固体全部变黑后,若立即停止通CO,则测得的样品中氧化铁的质量分数
考点:实验探究物质的组成成分以及含量,气体的净化(除杂),一氧化碳还原氧化铁,根据化学反应方程式的计算
专题:科学探究
分析:【问题讨论】
(1)从E装置中发生的反应是一氧化碳和氧化铁(红棕色)在高温下反应生成黑色的铁和二氧化碳去分析解答;
(2)从进入E中的气体是纯净、干燥的CO,就要除去混合气体中的二氧化碳和水分;先用装置中氢氧化钠溶液除去混合气体中的二氧化碳、再用石灰水检验混合气体中的二氧化碳是否除干净、最后用浓硫酸是除去水分去分析解答;
(3)从还要继续通往CO,以便让装置E中的产生二氧化碳全部进入F装置去分析解答;
(4)从由于利用称量F装置增加重量(二氧化碳)去计算参加反应的氧化铁的质量,故要外界防止外界空气(中CO2和水蒸气)进入F去分析解答;
(5)从反应物CO是空气污染物,在实验时要把剩余的CO除去去分析解答;
【数据处理】根据二氧化碳的质量求出氧化铁的质量分数.
【实验反思】从装置E中的产生二氧化碳没有进入F装置,会导致F增加质量减小,使二氧化碳质量偏小,导致计算得出氧化铁的质量分数减小去分析解答.
(1)从E装置中发生的反应是一氧化碳和氧化铁(红棕色)在高温下反应生成黑色的铁和二氧化碳去分析解答;
(2)从进入E中的气体是纯净、干燥的CO,就要除去混合气体中的二氧化碳和水分;先用装置中氢氧化钠溶液除去混合气体中的二氧化碳、再用石灰水检验混合气体中的二氧化碳是否除干净、最后用浓硫酸是除去水分去分析解答;
(3)从还要继续通往CO,以便让装置E中的产生二氧化碳全部进入F装置去分析解答;
(4)从由于利用称量F装置增加重量(二氧化碳)去计算参加反应的氧化铁的质量,故要外界防止外界空气(中CO2和水蒸气)进入F去分析解答;
(5)从反应物CO是空气污染物,在实验时要把剩余的CO除去去分析解答;
【数据处理】根据二氧化碳的质量求出氧化铁的质量分数.
【实验反思】从装置E中的产生二氧化碳没有进入F装置,会导致F增加质量减小,使二氧化碳质量偏小,导致计算得出氧化铁的质量分数减小去分析解答.
解答:解:【问题讨论】
(1)E装置中发生的反应是一氧化碳和氧化铁(红棕色)在高温下反应生成黑色的铁和二氧化碳,故答案为:样品由红色变成黑色;
(2)由草酸(H2C2O4)在浓硫酸作用下受热分解,化学方程式为H2C2O4
CO2↑+CO↑+H2O可知,由于进入E中的气体是纯净、干燥的CO,就要除去混合气体中的二氧化碳和水分;先用装置中氢氧化钠溶液除去混合气体中的二氧化碳、再用石灰水检验混合气体中的二氧化碳是否除干净、最后用浓硫酸是除去水分;故答案为:③;
(3)当E中固体完全反应后,还要继续通往CO,以便让装置E中的产生二氧化碳全部进入F装置,故答案为:E;
(4)由于利用称量F装置增加重量(二氧化碳)去计算参加反应的氧化铁的质量,故要外界防止外界空气(中CO2和水蒸气)进入F;故答案为:防止空气(中CO2和水蒸气)进入F;
(5)由于反应物CO是空气污染物,在实验时要把剩余的CO除去;故答案为:没有处理尾气装置;
【数据处理】解:设样品中氧化铁的质量分为X
Fe2O3+3CO
2Fe+3CO2
160 132
8.0g×x 4.4g
=
解之得:X=66.7%
故答案为:66.7%;
【实验反思】当观察到E中固体全部变黑后,若立即停止通CO,装置E中的产生二氧化碳没有进入F装置,会导致F增加质量减小,使二氧化碳质量偏小,导致计算得出氧化铁的质量分数减小;故答案为:偏小.
(1)E装置中发生的反应是一氧化碳和氧化铁(红棕色)在高温下反应生成黑色的铁和二氧化碳,故答案为:样品由红色变成黑色;
(2)由草酸(H2C2O4)在浓硫酸作用下受热分解,化学方程式为H2C2O4
| ||
| △ |
(3)当E中固体完全反应后,还要继续通往CO,以便让装置E中的产生二氧化碳全部进入F装置,故答案为:E;
(4)由于利用称量F装置增加重量(二氧化碳)去计算参加反应的氧化铁的质量,故要外界防止外界空气(中CO2和水蒸气)进入F;故答案为:防止空气(中CO2和水蒸气)进入F;
(5)由于反应物CO是空气污染物,在实验时要把剩余的CO除去;故答案为:没有处理尾气装置;
【数据处理】解:设样品中氧化铁的质量分为X
Fe2O3+3CO
| ||
160 132
8.0g×x 4.4g
| 160 |
| 132 |
| 8.0g×x |
| 4.0g |
解之得:X=66.7%
故答案为:66.7%;
【实验反思】当观察到E中固体全部变黑后,若立即停止通CO,装置E中的产生二氧化碳没有进入F装置,会导致F增加质量减小,使二氧化碳质量偏小,导致计算得出氧化铁的质量分数减小;故答案为:偏小.
点评:做题目时重点分析装置图中各装置的作用.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案
相关题目
下列应用的原理用化学方程式表示正确的是( )
| A、用适量的稀盐酸除铁锈 Fe2O3+6HCl=2FeCl2+3H2O | ||||
B、用一氧化碳作燃料 C0+02
| ||||
C、高温煅烧石灰石制取生石灰 CaC03
| ||||
D、用红磷燃烧测定空气中氧气含量 S+O2
|
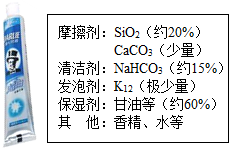 牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题.
牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题.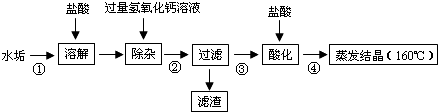
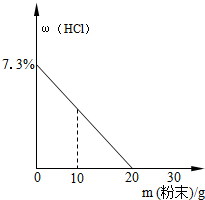 将混合均匀的Na2CO3和NaCl的粉末混合物不断加入100g稀盐酸中,溶液中HCl溶质的质量分数与加入粉末混合物的变化曲线如图所示.求:
将混合均匀的Na2CO3和NaCl的粉末混合物不断加入100g稀盐酸中,溶液中HCl溶质的质量分数与加入粉末混合物的变化曲线如图所示.求: 有些金属的氢氧化物有相似的化学性质,但物理性质却有所不同,如 Ca(OH)2、Ba(OH)2的溶解度就存在一定的差异,如表所示:
有些金属的氢氧化物有相似的化学性质,但物理性质却有所不同,如 Ca(OH)2、Ba(OH)2的溶解度就存在一定的差异,如表所示: 人类的生产、生活离不开金属.
人类的生产、生活离不开金属.