题目内容
在一定条件下,让置于密闭容器中的下列各组物质充分反应后(假设反应能进行到底),密闭容器中的剩余物质属于纯净物的是
A.质量比为1 : 8的O2和H2 B.质量比为3 : 5的C和O2
C.分子个数比为1 : 2的C和CO2 D.分子个数比为2 : 1的CO和O2
D

 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案如图所示实验操作中正确的是( )
|
| A. |
向试管中滴加液体 | B. |
给试管中液体加热 |
|
| C. |
称量一定质量的食盐 | D. |
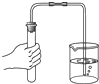
检查装置的气密性 |
阅读资料:
(1)氨气(NH3)具有还原性,可以还原氧化铜,生成铜、氮气和水;
(2)实验室制氨气:2NH4Cl + Ca(OH)2  CaCl2 + 2NH3↑ + 2H2O
CaCl2 + 2NH3↑ + 2H2O
(3)白色的无水硫酸铜遇水会变成蓝色,可以用于检测微量水的存在;
(4)碱石灰可以吸收水分,可以干燥氨气;
利用氨气还原氧化铜的反应,可设计测定铜元素相对原子质量近似值的实验。原理是先称量反应物氧化铜的质量,反应完全后测定生成物水的质量,由此计算铜元素相对原子质量。为此设计了下列实验装置(图中部分夹持仪器省略,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):
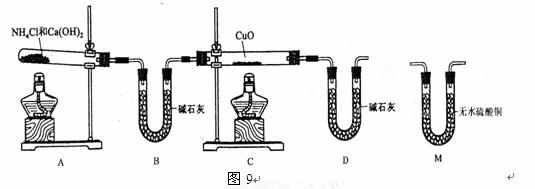
|
请回答下列问题
(1)写出氨气还原氧化铜的化学方程式
(2)B装置的作用是
D装置的作用是 __________
(3)为了确认没有水进入C装置中,需在整套装置中添加装置M于 (选填序号)。
a. A-B间 b. B-C间 c.C-D间
(4)在本实验中,若测得水的质量为a g,反应物氧化铜的质量为b g,则铜元素的相对原子质量是____。
(5)在本实验中,还可通过测定______和_____的质量,达到实验目的。
催化剂在化学反应中所起的作用是( )
|
| A. | 加快化学反应速率 | B. | 使生成物质量增加 |
|
| C. | 改变化学反应速率 | D. | 减慢化学反应速率 |
 C.Ba(OH)2+2HCl=BaCl2+2H2O D.NH4Cl NH3↑+HCl↑
C.Ba(OH)2+2HCl=BaCl2+2H2O D.NH4Cl NH3↑+HCl↑ A.向下排空气法 B.向上排空气法 C.排水法 D.以上方法都可以
A.向下排空气法 B.向上排空气法 C.排水法 D.以上方法都可以