题目内容
20.如图是实验室中常见气体制备、干燥、收集和性质实验的部分仪器装置图,请根据要求,回答下列问题: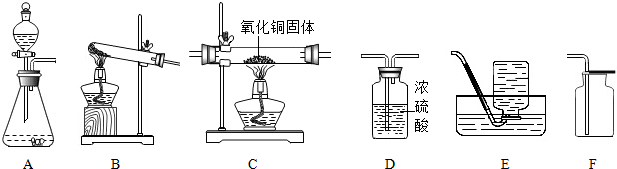
(1)实验室里,要用氯酸钾(KClO3)与二氧化锰混合加热,制备并收集一瓶干燥的氧气.
①所选仪器的连接顺序为BDF(填写仪器序号字母).
②发生反应的化学方程式为2KClO3 $\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
③该反应中,二氧化锰使氯酸钾的分解速度加快,反应结束后,欲从固体剩余物中提纯二氧化锰,通常的操作过程是溶解、过滤、洗涤、干燥
(2)用锌和稀硫酸反应制取氢气并进行氢气还原氧化铜的实验,若仪器C的大玻璃管观察到黑色粉末未变成红色,请写出该反应的化学方程式:H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.
分析 (1)氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法或排水法收集,生成的氧气用浓硫酸干燥;从固体剩余物中提纯二氧化锰的方法解答;
解答 解:(1)①装置是用来制取氧气的装置,由于浓硫酸具有吸水性,可以用来干燥气体,所以再通过浓硫酸把氧气干燥后再进行收集,由于要收集干燥的氧气,根据密度比空气大,用向上排空气法收集;
②氯酸钾制取氧气的方程式为:2KClO3 $\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
③氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,二氧化锰使氯酸钾的分解速度加快;因锰酸钾能溶于水,而二氧化锰不溶于水,因此可以用溶解、过滤除去,然后洗涤、干燥得到MnO2,所以反应后的固体剩余物中回收MnO2的主要操作步骤是溶解、过滤、洗涤、干燥;
(2)用锌和稀硫酸反应制取氢气并进行氢气还原氧化铜的实验,若仪器C的大玻璃管观察到黑色粉末未变成红色,请写出该反应的化学方程式:H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.
故答案为:(1)①BDF;②2KClO3 $\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;③氯酸钾的分解速度加快,溶解、过滤、洗涤、干燥;
(2)H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.
点评 本考点主要考查了仪器的连接和气体的除杂和干燥,同时也考查了化学方程式的书写,综合性比较强,本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
10.下列生活用品的主要成分属于有机合成材料的是( )
| A. | 木制茶几 | B. | 塑料脸盆 | C. | 羊毛围巾 | D. | 纯棉毛巾 |
8.掌握化学用语是学好化学的关键.下列化学用语及其表述的意义合理的是( )
①H2O-1个水分子 ②2Na+-2个钠离子 ③Cl+-氯离子 ④O2-2个氧原子
⑤MgO-氧化镁 ⑥2N-2个氮元素 ⑦He2-氦气中氦元素的化合价为1.
①H2O-1个水分子 ②2Na+-2个钠离子 ③Cl+-氯离子 ④O2-2个氧原子
⑤MgO-氧化镁 ⑥2N-2个氮元素 ⑦He2-氦气中氦元素的化合价为1.
| A. | ①②③⑤ | B. | ②③④⑤ | C. | ①②⑤⑦ | D. | ②⑤⑥⑦ |
5.济南市城市轨道交通的建设时全城人民的生活、工作环境更加便捷、美丽,下列做法中,不利于改善我市环境质量的是( )
| A. | 使用清洁能源代替煤和石油 | |
| B. | 提高城市道路机扫率,增加洒水频次,控制道路扬尘 | |
| C. | 提倡使用一次性发泡塑料餐具和塑料袋 | |
| D. | 全面禁止秸秆露天焚烧,加大秸秆综合利用力度 |
12.下列各组物质的鉴别中,所选的鉴别试剂,不正确的是( )
| 选项 | 待鉴别物质 | 鉴别试剂 |
| A | 氢氧化钠溶液和氢氧化钙溶液 | 二氧化碳 |
| B | 鉴别硫酸铵和硫酸钠固体 | 氢氧化钡溶液 |
| C | 食盐溶液和稀盐酸 | 紫色石蕊 |
| D | 氮气和二氧化碳气体 | 燃着的木条 |
| A. | A | B. | B | C. | C | D. | D |
9.下列有关概念的辨析中正确的是( )
| A. | 分子是保持所有物质化学性质的最小微粒 | |
| B. | 催化剂一定能加快化学反应的速率 | |
| C. | 元素的种类是由原子的中子数决定的 | |
| D. | 由一种元素组成的物质可能是混合物 |
10.我国地级及以上城市空气质量监测数据包括可吸入颗粒物(PM10)、细颗粒物(PM2.5)、SO2、NO2、O3和CO 6项指标,某同学对SO2、NO2、O3和CO四种物质的认识中不正确的是( )
| A. | O3属于单质 | B. | SO2、NO2和CO都属于氧化物 | ||
| C. | SO2、NO2中都含有氧分子 | D. | 四种物质中都含有氧元素 |
 氢氧化钙溶液和稀盐酸反应得到如图所示的pH曲线.
氢氧化钙溶液和稀盐酸反应得到如图所示的pH曲线.