题目内容
化学兴趣小组在进行酸、铖、盐的性质实验时,发现了一瓶氢氧化钠溶液未盖瓶塞,针对这一现象,该小组同学对这瓶溶液进行了如下探究:
【提出问题】
这瓶氢氧化钠溶液是否变质?若变质,变质程度如何?
【查阅资料】
a.氧氧化钠溶液会与二氧化碳发生化学反应.
b.氯化钡溶液呈中性,碳酸钠溶液呈碱性,两者能发生如下化学反应:
BaCl2十 Na2CO3═BaCO3+2NaCl
【作出猜想】
猜想一:该溶液没有变质,溶质是NaOH.
猜想二:该溶液完全变质,溶质是Na2CO3.
猜想三:该溶液部分变质,溶质是 .
【实验验证】
(1)为验证该溶液是否变质,小车和小华分别进行如下实验:
①小车取少许该溶液于试管中,滴加酚酞试液,溶液变红,于是得出“该溶液没有变质”的结论.’
②小华取少许该溶液于试管中,滴加稀盐酸,观察到 ,得出“该溶液已变质”的结论.
你认为 的结论正确.
(2)为验证该溶液的变质程度,小丽进行了如下实验:
取少许该溶液于试管中,加入过量的氯化钡溶液,产生白色沉淀,过滤后,在滤液中滴加酚酞试液,溶液变红,证明猜想三 (填“成立”或“不成立”).如果将氯化钡溶液换成氢氧化钡溶液,不能得出相同的结论,原因是 .
【交流反思】
氢氧化钠变质的原因是(用化学方程式表示): ,因此,氢氧化钠应 保存.
【提出问题】
这瓶氢氧化钠溶液是否变质?若变质,变质程度如何?
【查阅资料】
a.氧氧化钠溶液会与二氧化碳发生化学反应.
b.氯化钡溶液呈中性,碳酸钠溶液呈碱性,两者能发生如下化学反应:
BaCl2十 Na2CO3═BaCO3+2NaCl
【作出猜想】
猜想一:该溶液没有变质,溶质是NaOH.
猜想二:该溶液完全变质,溶质是Na2CO3.
猜想三:该溶液部分变质,溶质是
【实验验证】
(1)为验证该溶液是否变质,小车和小华分别进行如下实验:
①小车取少许该溶液于试管中,滴加酚酞试液,溶液变红,于是得出“该溶液没有变质”的结论.’
②小华取少许该溶液于试管中,滴加稀盐酸,观察到
你认为
(2)为验证该溶液的变质程度,小丽进行了如下实验:
取少许该溶液于试管中,加入过量的氯化钡溶液,产生白色沉淀,过滤后,在滤液中滴加酚酞试液,溶液变红,证明猜想三
【交流反思】
氢氧化钠变质的原因是(用化学方程式表示):
考点:药品是否变质的探究,碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:【作出猜想】:根据科学探究中提出猜想的方法进行猜想;
【实验验证】:(1)②如果溶液变质则溶液中存在的碳酸钠能够和稀盐酸反应生成气体,所以可加入稀盐酸溶液看是否有气泡冒出来判断溶液是否变质;
(2)若要证明是部分变质,则先检验有碳酸钠,可以加入过量氯化钡溶液,通过产生白色沉淀来证明,通过加入过量氯化钡溶液在除去碳酸钠之后检验溶液显碱性,说明还有氢氧化钠;如果将氯化钡溶液换成氢氧化钡溶液,不能得出相同的结论,原因是氢氧化钡显碱性,也能使酚酞试液变红;
【交流反思】:根据氢氧化钠固体暴露在空气中容易吸收水分而潮解,吸收空气中的二氧化碳而变质来思考.
【实验验证】:(1)②如果溶液变质则溶液中存在的碳酸钠能够和稀盐酸反应生成气体,所以可加入稀盐酸溶液看是否有气泡冒出来判断溶液是否变质;
(2)若要证明是部分变质,则先检验有碳酸钠,可以加入过量氯化钡溶液,通过产生白色沉淀来证明,通过加入过量氯化钡溶液在除去碳酸钠之后检验溶液显碱性,说明还有氢氧化钠;如果将氯化钡溶液换成氢氧化钡溶液,不能得出相同的结论,原因是氢氧化钡显碱性,也能使酚酞试液变红;
【交流反思】:根据氢氧化钠固体暴露在空气中容易吸收水分而潮解,吸收空气中的二氧化碳而变质来思考.
解答:解:
【作出猜想】:猜想是对可能的情况进行假设.猜想一:该瓶氢氧化钠溶液未变质,猜想二:该瓶氢氧化钠溶液完全变质,所以还有第三中情况就是部分变质,说明氢氧化钠还有剩余,故溶质是NaOH和Na2CO3;
【实验验证】:(1)②如果溶液变质则溶液中存在的碳酸钠能够和稀盐酸反应生成气体,所以可加入稀盐酸溶液看是否有气泡冒出来判断溶液是否变质;故小华的结论正确;
(2)若要证明是部分变质,则先检验有碳酸钠,可以加入过量氯化钡溶液,通过产生白色沉淀来证明,通过加入过量氯化钡溶液在除去碳酸钠之后检验溶液显碱性,说明还有氢氧化钠;如果将氯化钡溶液换成氢氧化钡溶液,不能得出相同的结论,原因是氢氧化钡显碱性,也能使酚酞试液变红;
【交流反思】:氢氧化钠固体暴露在空气中容易吸收水分而潮解,吸收空气中的二氧化碳而变质,化学方程式表示为:CO2+2NaOH=Na2CO3+H2O,因此,氢氧化钠应密封保存;
答案:【作出猜想】:NaOH和Na2CO3
【实验验证】:(1)②有气泡冒出 小华
(2)成立 氢氧化钡显碱性,也能使酚酞试液变红
交流反思】:CO2+2NaOH=Na2CO3+H2O 密封
【作出猜想】:猜想是对可能的情况进行假设.猜想一:该瓶氢氧化钠溶液未变质,猜想二:该瓶氢氧化钠溶液完全变质,所以还有第三中情况就是部分变质,说明氢氧化钠还有剩余,故溶质是NaOH和Na2CO3;
【实验验证】:(1)②如果溶液变质则溶液中存在的碳酸钠能够和稀盐酸反应生成气体,所以可加入稀盐酸溶液看是否有气泡冒出来判断溶液是否变质;故小华的结论正确;
(2)若要证明是部分变质,则先检验有碳酸钠,可以加入过量氯化钡溶液,通过产生白色沉淀来证明,通过加入过量氯化钡溶液在除去碳酸钠之后检验溶液显碱性,说明还有氢氧化钠;如果将氯化钡溶液换成氢氧化钡溶液,不能得出相同的结论,原因是氢氧化钡显碱性,也能使酚酞试液变红;
【交流反思】:氢氧化钠固体暴露在空气中容易吸收水分而潮解,吸收空气中的二氧化碳而变质,化学方程式表示为:CO2+2NaOH=Na2CO3+H2O,因此,氢氧化钠应密封保存;
答案:【作出猜想】:NaOH和Na2CO3
【实验验证】:(1)②有气泡冒出 小华
(2)成立 氢氧化钡显碱性,也能使酚酞试液变红
交流反思】:CO2+2NaOH=Na2CO3+H2O 密封
点评:检验氢氧化钠与碳酸钠的混合物时,可先把碳酸钠变成沉淀并且不生成影响氢氧化钠检验的碱性物质,然后使用酚酞检验氢氧化钠.

练习册系列答案
相关题目
下列关于试剂的取用的操作中,不正确的是( )
| A、用胶头滴管滴加少量试液试剂 |
| B、如果没有说明用量,取用固体只需盖满试管底部 |
| C、用镊子夹取块状固体 |
| D、实验室用剩的药品一定要放回试剂原瓶,不要乱仍乱放 |
再生产和科学研究中,需要用到一些保护气.当焊接金属时,为了隔绝空气,不能作为保护气的是( )
| A、氧气 | B、氮气 |
| C、二氧化碳 | D、稀有气体 |
下列关于物质组成和构成的说法错误的是( )
| A、酒精(C2H5OH)是由碳、氢、氧三种元素组成的 |
| B、过氧化氢(H2O2)分子是由水分子和氧原子构成的 |
| C、红磷和白磷都是由磷元素组成的单质 |
| D、水分子是由一个氧原子和2个氢原子构成的 |
在30℃时,50g水中最多溶解A物质5g,在60℃时20g水中最多能溶解B物质10g,则( )
| A、A的溶解度比B大 |
| B、B的溶解度比A大 |
| C、二者的溶解度相等 |
| D、无法比较 |
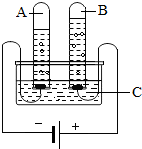 早在20世纪80年代,有一个叫王洪成的人制造了一个“水变油”的神话,他提出使用“高科技的添加剂”可使水变成汽油.那么水究竟能不能变成油呢?骗子往往披着科学的外衣,而科学可以给我们一双明辨是非的眼睛.同学们学习了水的组成知识后,不难用物质组成的观点揭穿这个骗局.
早在20世纪80年代,有一个叫王洪成的人制造了一个“水变油”的神话,他提出使用“高科技的添加剂”可使水变成汽油.那么水究竟能不能变成油呢?骗子往往披着科学的外衣,而科学可以给我们一双明辨是非的眼睛.同学们学习了水的组成知识后,不难用物质组成的观点揭穿这个骗局.