题目内容
9.在三个集气瓶中,分别盛有空气、氧气、二氧化碳,鉴别这三种气体的最好方法是( )| A. | 分别通入澄清的石灰水 | B. | 闻气味 | ||
| C. | 分别插入燃着的木条 | D. | 分别插入带火星的木条 |
分析 区别空气、氧气和二氧化碳三瓶无色气体,要求根据三种气体性质差别,所设计的方案能出现三种明显不同的实验现象,达到鉴别气体的目的.
解答 解:A、倒入澄清石灰水,石灰水变浑浊的气体为二氧化碳,无明显现象的为空气或氧气.无法区别空气和氧气,所以此方法不可行;故本选项错误;
B、空气、氧气和二氧化碳三种气体都是无味气体,所以闻气味不能将它们鉴别开来;故本选项错误;
C、燃着的木条分别放入瓶中,燃烧无明显变化的气体为空气;燃烧更旺的气体为氧气;燃烧熄灭的气体为二氧化碳;所以此方法简便可行;故本选项正确;
D、带火星的木条放入瓶中,木条复燃的是氧气,而在空气和二氧化碳中现象不明显,所以此方法不能将它们鉴别开来;故本选项错误;
故选C.
点评 本题考查了常见气体的鉴别,利用所要鉴别物质的性质差别,设计实验,实验中出现明显的现象差异,达到鉴别物质的目的.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.镁带在空气中充分燃烧后,会产生一些灰白色固体(以下简称A样品).为了弄清A样品的成分,小明、小亮、小红三位同学分别进行了如下实验探究:
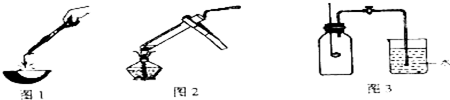
【实验与探究】
小明:(见图1)用分析天平称取三份经砂纸打磨的镁带,分别在空气中充分燃烧,待燃烧产物冷却后,称重.相关数据见下表
分析:2.4024g Mg在足量纯氧中燃烧,理论上应生成4.004g MgO.结合表中数据,可推断A样品中,除MgO外存在(填“存在”或“不存在”)其他物质.
小亮:(见图2)取少量A样品于试管中,加少量水,出现白色沉淀,微热,发现有使湿润的红色石蕊试纸变蓝的气体生成,则此气体是NH3 (填化学式)继续加足量水,仔细观察发现试管中除白色沉淀外,还有极少量的黑色不溶物.结合空气组成,小亮推测A样品应有MgO、Mg3N2 、C(填化学式)三种物质.
小红:(见图3)先用足量的红磷做燃烧实验,冷却后,打开止水阀,结果发现烧杯中的水倒流入广口瓶中,倒流入的水的体积与广口瓶容积之比约为$\frac{1}{5}$,此时瓶中剩余气体的主要成分为N2(填化学式);关闭止水阀,取出连带橡皮塞的燃烧匙,迅速塞上备用橡皮塞,向燃烧匙中加入镁带并引燃,取下备用橡皮塞,将燃烧匙迅速插入瓶中,并将橡皮塞塞紧,发现镁带继续燃烧,产生黄色火焰,冷却后,打开止水阀,结果发现烧杯中的水依然倒流入广口瓶中.小红的结论是镁带能在氮气中燃烧.
【交流与思考】
(1)小明的探究实验中,假如镁带未用砂纸打磨,则会不会给他的分析结果带来影响?请简述理由.
(2)综合上述探究,尝试写出镁条在空气中燃烧的有关化学方程式.
(3)若m克镁在空气中完全燃烧,共得到n克固体,则消耗O2的质量为(n-m)克.(计算时空气中的二氧化碳忽略不计)

【实验与探究】
小明:(见图1)用分析天平称取三份经砂纸打磨的镁带,分别在空气中充分燃烧,待燃烧产物冷却后,称重.相关数据见下表
| 反应前镁带的质量 | 反应的固体产物的质量 | |
| 第一次 | 2.4046g | 3.8854g |
| 第二次 | 2.4024g | 3.8839g |
| 第三次 | 2.4063g | 3.8857g |
小亮:(见图2)取少量A样品于试管中,加少量水,出现白色沉淀,微热,发现有使湿润的红色石蕊试纸变蓝的气体生成,则此气体是NH3 (填化学式)继续加足量水,仔细观察发现试管中除白色沉淀外,还有极少量的黑色不溶物.结合空气组成,小亮推测A样品应有MgO、Mg3N2 、C(填化学式)三种物质.
小红:(见图3)先用足量的红磷做燃烧实验,冷却后,打开止水阀,结果发现烧杯中的水倒流入广口瓶中,倒流入的水的体积与广口瓶容积之比约为$\frac{1}{5}$,此时瓶中剩余气体的主要成分为N2(填化学式);关闭止水阀,取出连带橡皮塞的燃烧匙,迅速塞上备用橡皮塞,向燃烧匙中加入镁带并引燃,取下备用橡皮塞,将燃烧匙迅速插入瓶中,并将橡皮塞塞紧,发现镁带继续燃烧,产生黄色火焰,冷却后,打开止水阀,结果发现烧杯中的水依然倒流入广口瓶中.小红的结论是镁带能在氮气中燃烧.
【交流与思考】
(1)小明的探究实验中,假如镁带未用砂纸打磨,则会不会给他的分析结果带来影响?请简述理由.
(2)综合上述探究,尝试写出镁条在空气中燃烧的有关化学方程式.
(3)若m克镁在空气中完全燃烧,共得到n克固体,则消耗O2的质量为(n-m)克.(计算时空气中的二氧化碳忽略不计)
1.除去下列物质中的杂质(括号内为杂质),所选试剂及操作方法均正确的一组是( )
| 选项 | 待提纯的物质 | 所选试剂及操作方法 |
| A | 氯化钠(碳酸钙) | 水、溶解、过滤、蒸发结晶 |
| B | 碳粉(铁) | 在空气中灼烧 |
| C | 氯化钾(氯酸钾) | 加入二氧化锰加热 |
| D | 硫酸铜(铁) | 加适量的水、过滤、蒸发结晶 |
| A. | A | B. | B | C. | C | D. | D |
19.分子、原子、离子都是构成物质的微粒,下列物质由分子构成的是( )
| A. | 黄金 | B. | 二氧化碳 | C. | 金刚石 | D. | 氯化钠 |
 蜡烛是由石蜡和棉线组成的.
蜡烛是由石蜡和棉线组成的.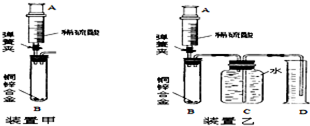 学习小组的同学在老师的帮助下对黄铜中铜和锌的含量展开探究.
学习小组的同学在老师的帮助下对黄铜中铜和锌的含量展开探究.